��Ŀ����
ij�о�С���һԪ�л�����HA���ܼ�����ˮ�Ļ����ϵ�е��ܽ�̶Ƚ����о�����25��ʱ������HA��ˮ�в��ֵ��룬��HAŨ��Ϊ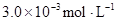 ʱ��������Ϊ0.20������ȣ��ѵ����HA������/��ʼHA���ܷ����������ڱ��в��ַ���˫�ۣ����ɣ�HA��2����ƽ����ϵ�У�һԪ�л�����HA���ܼ�����B����ˮ��W���еķ���ϵ��ΪK��K��C��HA��B��C��HA��W��1.0�����ﵽƽ����Է�����ʽ���ڵ�HA�ڱ���ˮ�����ܼ��еı���Ϊ1��1��������Ϣ���£�
ʱ��������Ϊ0.20������ȣ��ѵ����HA������/��ʼHA���ܷ����������ڱ��в��ַ���˫�ۣ����ɣ�HA��2����ƽ����ϵ�У�һԪ�л�����HA���ܼ�����B����ˮ��W���еķ���ϵ��ΪK��K��C��HA��B��C��HA��W��1.0�����ﵽƽ����Է�����ʽ���ڵ�HA�ڱ���ˮ�����ܼ��еı���Ϊ1��1��������Ϣ���£�
| 25��ƽ����ϵ | ƽ�ⳣ�� | �ʱ� | ��ʼ��Ũ�� |
��ˮ�У�HA 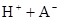 | 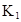 | 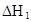 | 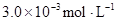 |
�ڱ��У�2HA 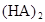 | 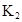 | 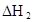 | 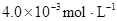 |
�ش��������⣺
��1������25��ʱˮ��Һ��HA�ĵ���ƽ�ⳣ��K1��___________��
��2��25�棬��ˮ��Һ��pHΪ___________������֪��1g2��0.3��lg3��0.5���ڱ���ϵ��HA��ת����Ϊ___________��
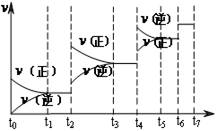
��3���ڱ��У�HA�������ۣ�2HA
 ��HA��2����Ӧ�ڽϵ��¶����Է����У���
��HA��2����Ӧ�ڽϵ��¶����Է����У���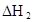 ___________0��
___________0����4��25������ϵ�У�HA�ڱ��з������ۣ������ijʱ����Һ����Ũ������
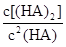 ��130����Ӧ��___________������С�
��130����Ӧ��___________������С�
��1��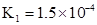 mol/L ��2��3.2�� 40% ��3���� ��4����
mol/L ��2��3.2�� 40% ��3���� ��4����
���������������1��HA��ˮ��Һ�е��룺HA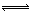 H++A-�����ݵ����Ϊ0.20��c��H+��=3.0��10-3mol/L��0.20=6.0��10-4mol?L?1����K=6.0��10-4mol?L?1��6.0��10-4mol?L?1�£�3.0��10-3mol?L?1��6.0��10-4mol?L?1��=1.5��10-4mol?L?1����2��pH=-lg��H+��=-lg��6.0��10-4��=3.2���ﵽƽ����Է�����ʽ���ڵ�HA�ڱ���ˮ�����ܼ��еı���Ϊ1��1��c��HA��=3.0��10-3mol?L?1��6.0��10-4mol?L?1=2.4��10-3mol?L?1��ת����HAΪ4.0��10-3mol?L?1��2.4��10-3mol?L?1=1.6��10-3mol?L?1�������ڱ���ϵ��HA��ת����Ϊ,1.6��10-3mol?L?��4.0��10-3mol?L?1��100% ="40%" ����3���÷�Ӧ�ڽϵ��¶����Է����У�T��Сʱ��?H-T?S<0����Ϊ��Ӧ���ʵ�����С����?S<0������?H<0����4���ɣ�2�������ݿ����2HA
H++A-�����ݵ����Ϊ0.20��c��H+��=3.0��10-3mol/L��0.20=6.0��10-4mol?L?1����K=6.0��10-4mol?L?1��6.0��10-4mol?L?1�£�3.0��10-3mol?L?1��6.0��10-4mol?L?1��=1.5��10-4mol?L?1����2��pH=-lg��H+��=-lg��6.0��10-4��=3.2���ﵽƽ����Է�����ʽ���ڵ�HA�ڱ���ˮ�����ܼ��еı���Ϊ1��1��c��HA��=3.0��10-3mol?L?1��6.0��10-4mol?L?1=2.4��10-3mol?L?1��ת����HAΪ4.0��10-3mol?L?1��2.4��10-3mol?L?1=1.6��10-3mol?L?1�������ڱ���ϵ��HA��ת����Ϊ,1.6��10-3mol?L?��4.0��10-3mol?L?1��100% ="40%" ����3���÷�Ӧ�ڽϵ��¶����Է����У�T��Сʱ��?H-T?S<0����Ϊ��Ӧ���ʵ�����С����?S<0������?H<0����4���ɣ�2�������ݿ����2HA ��HA��2��ƽ�ⳣ��K=8.0��10-4mol?L?1�£�2.4��10-3mol?L?1��2=146��
��HA��2��ƽ�ⳣ��K=8.0��10-4mol?L?1�£�2.4��10-3mol?L?1��2=146��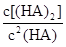 ��130<K�����Է�Ӧ������Ӧ������С�
��130<K�����Է�Ӧ������Ӧ������С�
���㣺���⿼��ƽ�ⳣ���ļ����Ӧ�á�pH��ת���ʵļ��㡢��Ӧ�Է����еķ�����

 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д���һ���������İ�������粒����������Ƶ��ܱ���������У���������������䣬��������������Բ��ƣ����ں㶨�¶���ʹ��ﵽ�ֽ�ƽ�⣺NH2COONH4��s��  2NH3��g����CO2��g��
2NH3��g����CO2��g��
ʵ���ò�ͬ�¶��µ�ƽ�����������±���
| �¶�/�� | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| ƽ����ѹ ǿ/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| ƽ��������Ũ��/mol�� L��1 | 2.4�� 10��3 | 3.4�� 10��3 | 4.8�� 10��3 | 6.8�� 10��3 | 9.4�� 10��3 |
��1�������жϸ÷ֽⷴӦ�Ѿ��ﵽƽ�����________��
A��2v��NH3����v��CO2��
B���ܱ���������ѹǿ����
C���ܱ������л��������ܶȲ���
D���ܱ������а����������������
��2�����ݱ������ݣ���ʽ����25.0 ��ʱ�ķֽⷴӦƽ�ⳣ����_______________��
��3��ȡһ�����İ�������粒������һ�����������ܱ���������У���25.0 ���´ﵽ�ֽ�ƽ�⡣���ں�����ѹ�������������������粒����������________������ӡ��������١����䡱����
һ���¶��£���2L�ܱ�������NO2��O2�ɷ������з�Ӧ�� 4NO2(g)+O2(g)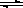 2N2O5(g)+5286 kJ��֪��ϵ��n(NO2)��ʱ��仯���±���
2N2O5(g)+5286 kJ��֪��ϵ��n(NO2)��ʱ��仯���±���
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
��1����˵���÷�Ӧ�Ѵﵽƽ��״̬���� ��
A��v��NO2��=4v��O2�� B��������ѹǿ���ֲ���
C��v����N2O5��=2v����O2�� D���������ܶȱ��ֲ���
��2����Ӧ�ﵽƽ���NO2��ת����Ϊ ���� ʱ����ͨ��һ������������NO2��ת���ʽ� (���������С���������䡱)��
��3��ͼ���ܱ�ʾN2O5��Ũ�ȱ仯�������� ����O2��ʾ��0~500s�ڸ÷�Ӧ��ƽ������v= ��
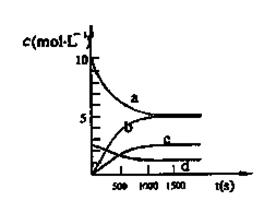
��4����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ������Ӧ�����ƶ����� ��
A����ʱ�����NO2���� B���ʵ������¶�
C������O2��Ũ�� D��ѡ���Ч����
������̶����ܱ������У��������»�ѧ��Ӧ��N2O4��g�� 2NO2��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
2NO2��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
| t /�� | 80 | 100 | 120 |
| K | 1.80 | 2.76 | 3.45 |
��ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK�� ��
��2���÷�ӦΪ ��Ӧ������ȡ����ȡ�����
��3���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�������� ��
A�������ڻ�������ܶȲ���
B�����������c��NO2������
C��0.5mol N2O4�ֽ��ͬʱ��1 mol NO2����
��4����80��ʱ����2.80molN2O4�������2L�̶��ݻ����ܱ������У�һ��ʱ���Ը������ڵ����ʽ��з������õ��������ݣ�
  | 0 | 20 | 40 | 60 | 80 | 100 |
| n��N2O4�� | 2.80 | A | 2.00 | c | d | 1.60 |
| n��NO2�� | 0 | 0.96 | b | 2.08 | 2.40 | 2.40 |
��b��ֵΪ ��
��N2O4��ƽ��ת����Ϊ ��
��20s��40s����N2O4��ʾ��ƽ����Ӧ���ʦԣ�N2O4���� ��
��ѧ��Ӧԭ���ڿ��к��������й㷺Ӧ�á�
����ͼװ����ʾ��A��B�еĵ缫Ϊ��Ķ��Ե缫��C��DΪ���ڽ���Na2SO4��Һ����ֽ���ϵIJ��У���Դ��a��b��������A��B�г���KOH��Һ������KOH��Һ��ˮ���С��ж�K1���պ�K2��K3ֱͨ���硣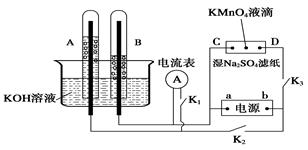
�ش��������⣺
��1�� a�ǵ�Դ�� ����д��A�еĵ缫��ӦʽΪ_____��
��2��ʪ��Na2SO4��ֽ�����ܹ۲쵽��������____________��
��3�����һ��ʱ���A��B�о��������Χ�缫������ʱ�ж�K2��K3���պ�K1�����ֵ�������ָ���ƶ���д����ʱB�еĵ缫��ӦʽΪ ��
�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ��һ��������з�Ӧ�ϳɼ״���CO(g)��2H2(g)  CH3OH(g) ��H���±����������Ǹ÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)����ش��������⣺
CH3OH(g) ��H���±����������Ǹ÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)����ش��������⣺
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
��4���ɱ��������жϦ�H 0�����������������������
��5�������������䣬ֻ�ı�����һ�����������д�ʩ����״����ʵ��� ��
A�������¶ȣ�B��ʹ�ú��ʵĴ�����C����С�������ݻ���D�����������H2��E����ѹʱ������He��F������ϵ�з����CH3OH
��6��ij�¶��£���2mol CO��6 mol H2����2L�ܱ������У���Ӧ���е�4minĩ�ﵽƽ�⣬��ʱ���c(CO) ��0.2 mol/L ����0~4min��H2�ķ�Ӧ����Ϊ ���������¶��ݻ������������г���һ������CH3OH�����´ﵽ��ѧƽ��״̬����ԭƽ��״̬��ȣ���ʱƽ����������CH3OH��������� ����������С�������䡱����
ijС������H2C2O4��Һ������KMnO4��Һ��Ӧ��̽������������Ի�ѧ��Ӧ���ʵ�Ӱ�족��ʵ��ʱ���ȷֱ���ȡ������Һ��Ȼ�����Թ���Ѹ����Ͼ��ȣ���ʼ��ʱ��ͨ���ⶨ��ɫ����ʱ�����жϷ�Ӧ�Ŀ�������С����������·�����
| ʵ���� | H2C2O4��Һ | ����KMnO4��Һ | �¶� | ||
| Ũ��(mol·L��1) | ���(mL) | Ũ��(mol·L��1) | ��� (mL) | ||
| �� | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| �� | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| �� | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
��1����֪��Ӧ��H2C2O4ת��ΪCO2�ݳ���KMnO4ת��ΪMnSO4��ÿ����1molH2C2O4ת��_______mol���ӡ�Ϊ�˹۲쵽��ɫ��ȥ��H2C2O4��KMnO4��ʼ�����ʵ�����Ҫ����Ĺ�ϵΪn(H2C2O4)��n(KMnO4)��______��
��2��̽���¶ȶԻ�ѧ��Ӧ����Ӱ���ʵ������________(���ţ���ͬ)����̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ����Ӱ���ʵ������________��
��3��ʵ��ٲ��KMnO4��Һ����ɫʱ��Ϊ40s�����Ի��ǰ����Һ�����С�仯�����ʱ����ƽ����Ӧ����v(KMnO4)��________mol·L��1·min��1��
��4����֪ʵ�����c(MnO4-)����Ӧʱ��t�ı仯��������ͼ�������������������䣬����ͼ�л���ʵ�����c(MnO4-)��t�ı仯����ʾ��ͼ��
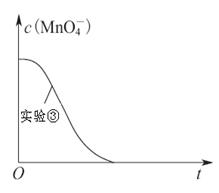
��7�֣��ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɶ����ѵ����ȼ�ϣ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У�
��CH4��g��+H2O��g��?CO��g��+3H2��g����H1=+206��1kJ/mol
��CH4��g��+CO2��g��?2CO��g��+2H2��g����H2=+247��3kJ/mol
��CO��g��+H2O��g��?CO2��g��+H2��g����H3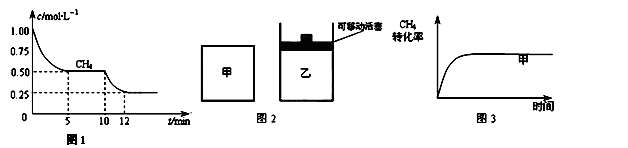
��ش��������⣺
��1����һ�����ܱ������н��з�Ӧ�٣����CH4�����ʵ���Ũ���淴Ӧʱ��ı仯��ͼ1��ʾ����Ӧ���е�ǰ5min�ڣ� ��H2��= ��10minʱ���ı��������������� ��
��H2��= ��10minʱ���ı��������������� ��
��2����ͼ2��ʾ���ڼס����������зֱ��������ʵ�����CH4��CO2��ʹ�ס�����������ʼ�ݻ���ȣ�����ͬ�¶��·�����Ӧ�ڣ���ά�ַ�Ӧ�������¶Ȳ��䣮��֪��������CH4��ת������ʱ��仯��ͼ����ͼ3��ʾ������ͼ3�л�����������CH4��ת������ʱ��仯��ͼ��
��3����Ӧ���С�H3= ��800��ʱ����Ӧ�۵Ļ�ѧƽ�ⳣ��K=1��0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ������±���
| CO | H2O | CO2 | H2 |
| 0��5mol | 8��5mol | 2��0mol | 2��0mol |
��ʱ��Ӧ���������淴Ӧ���ʵĹ�ϵʽ�� ������ţ���
a��v��������v���棩 b��v��������v���棩
c��v������=v���棩 d�����жϣ�

 b��
b�� c��
c�� d��HI
d��HI �����ʵ�����ʱ��ı仯��ͼ��ʾ��0~2min�ڵ�ƽ����Ӧ����
�����ʵ�����ʱ��ı仯��ͼ��ʾ��0~2min�ڵ�ƽ����Ӧ���� _________��
_________��
 b��
b�� c��
c�� d��
d��
 Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)