题目内容
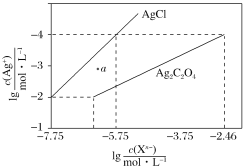
【题目】常温下,用AgNO3溶液分别滴定浓度均为0.01mol·L-1的KCl、K2C2O4溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O42-的水解)。下列叙述正确的是( )
A.Ksp(Ag2C2O4)=10-7
B.a点表示的是AgCl的不饱和溶液
C.向c(Cl-)=c(C2O42-)=0.1mol·L-1的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀
D.Ag2C2O4(s)+2Cl-(aq)![]() 2AgCl(s)+C2O42-(aq)的平衡常数为109.04
2AgCl(s)+C2O42-(aq)的平衡常数为109.04
【答案】D
【解析】
A.Ksp(Ag2C2O4)=c2(Ag+)·c(C2O![]() )=(10-4)2×(10-2.46)=10-10.46,故A错误;
)=(10-4)2×(10-2.46)=10-10.46,故A错误;
B.在a点,c(Ag+)大于平衡浓度,故a点的浓度积Qc(AgCl)>Ksp(AgCl),故为氯化银的过饱和溶液,将有沉淀析出,故B错误;
C.根据图像可知,当阴离子浓度相同时,生成AgCl沉淀所需的c(Ag+)小,故向c(Cl-)=c(C2O![]() )的混合液中滴入AgNO3溶液时,先析出氯化银沉淀,故C错误;
)的混合液中滴入AgNO3溶液时,先析出氯化银沉淀,故C错误;
D.Ag2C2O4(s)+2Cl-(aq)![]() 2AgCl(s)+C2O42- (aq)的平衡常数K=
2AgCl(s)+C2O42- (aq)的平衡常数K=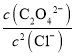 ,此时溶液中的c(Ag+)相同,故有:K=
,此时溶液中的c(Ag+)相同,故有:K= =
=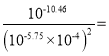 109.04,故D正确;
109.04,故D正确;
选D。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案【题目】铜的化合物在工农业生产中具有重要地位。请按要求回答下列问题。
Ⅰ.纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
方法a | 用葡萄糖还原新制的Cu(OH)2(NaOH过量)制备Cu2O |
方法b | 用肼(N2H4)加热还原新制的Cu(OH)2制备Cu2O,同时放出N2 |
方法c | 用炭粉在1000℃以上还原CuO制备Cu2O,同时放出CO |
(1)写出方法a的化学方程式:__。
(2)已知:①2Cu(s)+![]() O2(g)=Cu2O(s) △H=-169kJ·mol﹣1
O2(g)=Cu2O(s) △H=-169kJ·mol﹣1
②C(s)+![]() O2(g)=CO(g) △H=-110.5kJ·mol﹣1
O2(g)=CO(g) △H=-110.5kJ·mol﹣1
③CuO(s)=Cu(s)+![]() O2(g) △H=+157kJ·mol﹣1
O2(g) △H=+157kJ·mol﹣1
写出方法c反应的热化学方程式:__。
(3)在相同的密闭容器中,用上表方法制得的三种Cu2O分别进行催化分解水的实验:2H2O(g)![]() 2H2(g)+O2(g) △H>0。水蒸气的浓度随时间t变化如下表所示:
2H2(g)+O2(g) △H>0。水蒸气的浓度随时间t变化如下表所示:
序号 | 0 | 10 | 20 | 30 | 40 | 50 | |
i | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 | ii | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
iii | T2 | 0.100 | 0.0960 | 0.0930 | 0.0900 | 0.0900 | 0.0900 |
对比上述实验数据,可获得的结论:
①催化剂的催化效率:实验i___实验ii(填“>”“<”“=”,下同)。
②T1__T2。
Ⅱ.在2L的恒温密闭容器中通入5molO2并加入足量Cu2S发生反应:Cu2S(s)+O2(g)=2Cu(s)+SO2(g) △H1=-271.4kJ/mol,
反应过程中某气体的体积分数随时间变化如图所示。
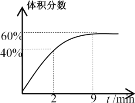
(4)反应前2min平均反应速率v(SO2)=__;该温度下反应的平衡常数K=__。
若保持温度不变向平衡体系中再通入1molO2,达到新平衡后氧气的体积分数__(填“大于”“小于”或“等于”)原平衡时氧气的体积分数。
【题目】某同学研究浓度对化学平衡的影响,下列说法正确的是
已知:Cr2O72-(aq)(橙色)+H2O(l) | |
步骤: | 现象: 待试管b中颜色不变后与试管a比较, 溶液颜色变浅。 滴加浓硫酸,试管c温度略有升高, 溶液颜色与试管a相比,变深。 |
A. 该反应是一个氧化还原反应
B. 待试管b中溶液颜色不变的目的是使Cr2O72-完全反应
C. 该实验不能证明减小生成物浓度,平衡正向移动
D. 试管c中的现象说明影响平衡的主要因素是温度