题目内容
【题目】铜的化合物在工农业生产中具有重要地位。请按要求回答下列问题。
Ⅰ.纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
方法a | 用葡萄糖还原新制的Cu(OH)2(NaOH过量)制备Cu2O |
方法b | 用肼(N2H4)加热还原新制的Cu(OH)2制备Cu2O,同时放出N2 |
方法c | 用炭粉在1000℃以上还原CuO制备Cu2O,同时放出CO |
(1)写出方法a的化学方程式:__。
(2)已知:①2Cu(s)+![]() O2(g)=Cu2O(s) △H=-169kJ·mol﹣1
O2(g)=Cu2O(s) △H=-169kJ·mol﹣1
②C(s)+![]() O2(g)=CO(g) △H=-110.5kJ·mol﹣1
O2(g)=CO(g) △H=-110.5kJ·mol﹣1
③CuO(s)=Cu(s)+![]() O2(g) △H=+157kJ·mol﹣1
O2(g) △H=+157kJ·mol﹣1
写出方法c反应的热化学方程式:__。
(3)在相同的密闭容器中,用上表方法制得的三种Cu2O分别进行催化分解水的实验:2H2O(g)![]() 2H2(g)+O2(g) △H>0。水蒸气的浓度随时间t变化如下表所示:
2H2(g)+O2(g) △H>0。水蒸气的浓度随时间t变化如下表所示:
序号 | 0 | 10 | 20 | 30 | 40 | 50 | |
i | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 | ii | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
iii | T2 | 0.100 | 0.0960 | 0.0930 | 0.0900 | 0.0900 | 0.0900 |
对比上述实验数据,可获得的结论:
①催化剂的催化效率:实验i___实验ii(填“>”“<”“=”,下同)。
②T1__T2。
Ⅱ.在2L的恒温密闭容器中通入5molO2并加入足量Cu2S发生反应:Cu2S(s)+O2(g)=2Cu(s)+SO2(g) △H1=-271.4kJ/mol,
反应过程中某气体的体积分数随时间变化如图所示。
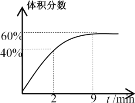
(4)反应前2min平均反应速率v(SO2)=__;该温度下反应的平衡常数K=__。
若保持温度不变向平衡体系中再通入1molO2,达到新平衡后氧气的体积分数__(填“大于”“小于”或“等于”)原平衡时氧气的体积分数。
【答案】CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH![]() CH2OH(CHOH)4COONa+Cu2O↓+3H2O C(s)+2CuO(s)
CH2OH(CHOH)4COONa+Cu2O↓+3H2O C(s)+2CuO(s)![]() Cu2O(s)+CO(g) △H=+34.5kJ·mol-1 < < 0.5mol/(L·min) 1.5 等于
Cu2O(s)+CO(g) △H=+34.5kJ·mol-1 < < 0.5mol/(L·min) 1.5 等于
【解析】
根据盖斯定律书写热化学方程式并进行反应热的计算;根据表格数据判断达到平衡的时间从而判断催化效率;根据图像分析得出该图像表示SO2的体积分数随时间的变化,结合三段式计算反应速率和平衡常数,根据等效平衡的概念分析解答。
(1)方法a用葡萄糖还原新制的Cu(OH)2(NaOH过量)制备Cu2O,反应的化学方程式为CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH![]() CH2OH(CHOH)4COONa+Cu2O↓+3H2O,故答案为:CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH
CH2OH(CHOH)4COONa+Cu2O↓+3H2O,故答案为:CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH![]() CH2OH(CHOH)4COONa+Cu2O↓+3H2O;
CH2OH(CHOH)4COONa+Cu2O↓+3H2O;
(2)方法c用炭粉在1000℃以上还原CuO制备Cu2O,同时放出CO,反应的化学方程式为C(s)+2CuO(s)![]() Cu2O(s)+CO(g),可通过反应①+②-2③得到,则根据盖斯定律可得ΔH=(-169kJ·mol﹣1)+(-110.5kJ·mol﹣1)-2(+157kJ·mol﹣1)=+34.5kJ·mol﹣1,故答案为:C(s)+2CuO(s)
Cu2O(s)+CO(g),可通过反应①+②-2③得到,则根据盖斯定律可得ΔH=(-169kJ·mol﹣1)+(-110.5kJ·mol﹣1)-2(+157kJ·mol﹣1)=+34.5kJ·mol﹣1,故答案为:C(s)+2CuO(s)![]() Cu2O(s)+CO(g) △H=+34.5kJ·mol-1;
Cu2O(s)+CO(g) △H=+34.5kJ·mol-1;
(3)①根据表格数据分析可知,实验ⅱ更快达到平衡状态,反应速率更快,故催化效率实验i<实验ii,故答案为:<;
②比较实验ii、ⅲ,实验ⅲ中初始水蒸气浓度是实验ii的一倍,但反应结束时水蒸气的浓度小于实验2的一倍,故平衡向正反应反应移动,该反应为吸热反应,升高温度,平衡向吸热方向移动,则T1<T2,故答案为:<;
(4)根据图示可知曲线为SO2的体积分数,反应过程中气体体积不变,则2min时,生成SO2的物质的量为n=5mol×40%=2mol,则2min平均反应速率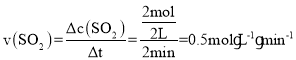 ,反应在9min后达到平衡,此时SO2的体积分数为60%,则n(SO2)=5×60%=3mol,n(O2)=5×40%=2mol,则平衡常数
,反应在9min后达到平衡,此时SO2的体积分数为60%,则n(SO2)=5×60%=3mol,n(O2)=5×40%=2mol,则平衡常数 ,该反应前后体积不变,则通入氧气时,平衡不移动,转化率不变,则氧气的体积分数等于原平衡时氧气的体积分数,故答案为:0.5 mol/(L·min);1.5;等于。
,该反应前后体积不变,则通入氧气时,平衡不移动,转化率不变,则氧气的体积分数等于原平衡时氧气的体积分数,故答案为:0.5 mol/(L·min);1.5;等于。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案