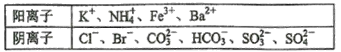题目内容
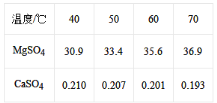
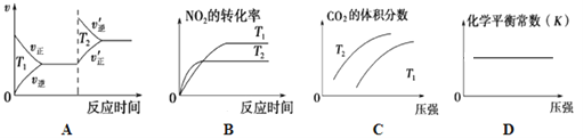
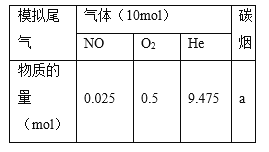
【题目】在一定温度下,将气体 X和气体Y各0.16mol充入 10L恒容密闭容器中,发生反应: X(g) + Y(g) 2Z(g) △ H < 0.一段时间后达到平衡,反应过程中测定的数据如表,下列说法正确的是( )

A.反应前 2 min 的平均速率v(Z) > 2.0 × 103 mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前:v(逆) > v(正)
C.保持其他条件不变,起始时向容器中充入0.32 mol气体 X和0.32 mol气体Y,到达平衡时,c(Z) > 0.24 mol·L-1
D.该温度下此反应的平衡常数:K = 1.44
【答案】D
【解析】
A选项,反应前 2 min 内Y的改变量为0.04mol,则Z改变量为0.02mol,2min内Z的平均速率![]() ,故A错误;
,故A错误;
B选项,其他条件不变,降低温度,平衡向放热方向移动,正向移动,反应达到新平衡前:v(正) > v(逆),故B错误;
C选项,充入气体 X和气体Y各0.16mol,平衡时Y的物质的的量为0.10mol,则改变量为0.06mol,此时Z的物质的量为0.12mol,浓度为0.012molL-1,保持其他条件不变向容器中充入0.32 mol气体 X和0.32 mol气体Y,用建模思想,相当于两个容器,缩小容器加压,平衡不移动,浓度为原来2倍,即c(Z) = 0.024 mol·L-1,故C错误;
D选项,平衡时,Y的物质的量为0.1mol,X的物质的量为0.1mol,Z的物质的量为0.12mol,该温度下此反应的平衡常数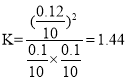 ,故D正确。
,故D正确。
综上所述,答案为D。

 名校课堂系列答案
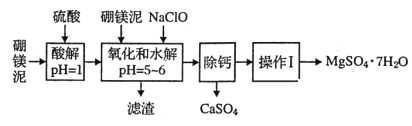
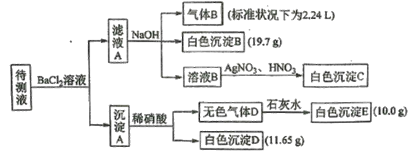
名校课堂系列答案【题目】某地环保部门将收集到的一定量酸雨试样分成甲、乙、丙、丁四份,进行如图所示的实验探究。
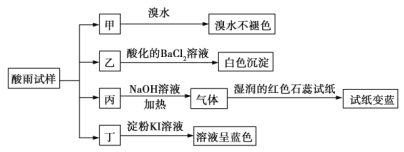
已知酸雨试样中可能含有下表所示的某些离子:
阳离子 |
|
阴离子 |
|
请回答下列问题:
(1)![]() 是______,
是______,![]() 是______。
是______。
(2)可能存在的阴离子是______,能证明该阴离子是否存在的简单实验操作为______。
(3)写出丁试样中滴加淀粉![]() 溶液所发生反应的离子方程式:______。
溶液所发生反应的离子方程式:______。
(4)某次降雨收集到![]() 雨水,向雨水中滴加
雨水,向雨水中滴加![]() 的
的![]() 溶液,充分反应后测得溶液中
溶液,充分反应后测得溶液中![]() ,再向该溶液中加入足量的
,再向该溶液中加入足量的![]() 溶液,经过滤、蒸干、称重,测得沉淀的质量为
溶液,经过滤、蒸干、称重,测得沉淀的质量为![]() 。假设雨水的酸性仅由
。假设雨水的酸性仅由![]() 和
和![]() 的排放所致,则排放到空气中的
的排放所致,则排放到空气中的![]() 和
和![]() 的物质的量之比约为______(不考虑
的物质的量之比约为______(不考虑![]() 的相互反应)。
的相互反应)。