��Ŀ����
����Ŀ��������N2H4��������������һ����Ҫ�Ļ��ȼ�ϣ�N2H4��N2O4�ܷų��������ȡ�
��1����֪��2NO2(g)��N2O4(g) ��H����57.20kJ��mol��1��һ���¶��£����ܱ������з�Ӧ2NO2(g)��N2O4(g) �ﵽƽ�⡣������������ʱ�����д�ʩ��
A����СNO2��Ũ�� B�������¶� C������NO2��Ũ�� D�������¶�
�����NO2ת���ʵ���_______������ĸ����
��2��25��ʱ��1.00gN2H4(l)������N2O4(l)��ȫ��Ӧ����N2(g)��H2O (l) ���ų�19.14kJ
����������Ӧ2N2H4(l)+N2O4(l)��3N2(g)+4H2O (l)����H��______kJ��mol��1��
��3��17����1.01��105Pa���ܱ�������N2O4��NO2�Ļ������ﵽƽ��ʱ��c(NO2)��0.0300mol��L��1��c(N2O4)��0.0120mol��L��1�����㷴Ӧ2 NO2(g)![]() N2O4(g)��ƽ�ⳣ��K=______��
N2O4(g)��ƽ�ⳣ��K=______��
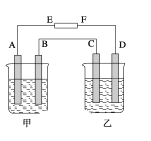
��4������һ������Cu ��������ŨHNO3��Ӧ���Ƶ�1.00L�Ѵ�ƽ���N2O4��NO2
������壨17����1.01��105Pa��������������������Cu��������________��
���𰸡�BC ��1224.96 13.3 1.73g
��������
��1�����ڸ÷�ӦΪ���������С�ķ��ȷ�Ӧ��Ҫ���NO2ת���ʣ���Ӧ�ò�ȡ���������¶ȣ�������NO2��Ũ�ȣ�������ѹǿ�ȴ�ʩ������B��C����Ҫ��
��2����1.00gN2H4(l)�ų�19.14kJ����2mol(��64g)N2H4(l)����Ϊ1224.96kJ��������H��1224.96kJ��mol��1��
��3������������֪��ƽ��ʱc(N2O4)��0.0120mol��L��1��c(NO2)��0.0300mol��L��1��K��c(N2O4)/c2(NO2) ��0.0120/0.0300��0.0300 ��13.3��
��4���ɣ�3����֪����17����1.01��105Pa�ﵽƽ��ʱ��1.00L��������У�n(N2O4)��c(N2O4)��V��0.0120mol��L��1��1.00L��0.0120mol��n(NO2)��c(NO2)��V��0.0300mol��L��1��1.00L��0.0300mol����n��(NO2)��n(NO2)��2��n(N2O4)��0.0540mol����Cu��4HNO3��Cu(NO3)2��2NO2����2H2O�ɵã�m(Cu)�� 64g��mol��1��0.0540mol/2 ��1.73g��

 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�