题目内容
【题目】化学兴趣小组设定以下实验方案,测定某已变质为碳酸钠的小苏打样品中NaHCO3的质量分数。
方案一:称取一定质量样品,置于坩埚中加热至恒重,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为:__________________;
(2)实验中需加热至恒重的目的是:_________________________;
方案二:称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤,干燥沉淀,称量固体质量,计算。
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为_________________;
(2)实验中判断沉淀是否完全的方法是_______________________________。
方案三:按如图装置进行实验:

(1)B装置内所盛试剂是__________ 分液漏斗中____________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.9g样品,实验后测得C装置增重8.8g,则样品中NaHCO3的质量分数为____________________。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是__________________________________。
【答案】2NaHCO3![]() Na2CO3+H2O+CO2↑保证NaHCO3分解完全玻璃棒取少量上层清液于试管中,滴加一滴Ba(OH)2溶液,观察是否有白色沉淀生成浓硫酸不能70.4%(70%)缺少一套将A、B装置内的CO2气体驱赶到C装置中的装置
Na2CO3+H2O+CO2↑保证NaHCO3分解完全玻璃棒取少量上层清液于试管中,滴加一滴Ba(OH)2溶液,观察是否有白色沉淀生成浓硫酸不能70.4%(70%)缺少一套将A、B装置内的CO2气体驱赶到C装置中的装置
【解析】
[方案一]碳酸氢钠不稳定,受热易分解,根据加热前后固体质量变化,根据差量法求碳酸氢钠的质量,进而求得碳酸钠的质量分数。
(1)碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;
(2)加热恒重保证碳酸氢钠完全分解;
[方案二]碳酸钠和碳酸氢钠都和氢氧化钡反应生成碳酸钡沉淀,根据生成沉淀的质量来计算碳酸钠的质量分数。
(1)根据过滤操作考虑所需仪器;
(2)可取上层清液,继续加沉淀剂,看是否生成沉淀;
[方案三]
(1)由测定含量的实验可以知道,A中发生Na2CO3+H2SO4=Na2SO4+H2O+CO2↑、2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑,B中为浓硫酸吸收水,干燥二氧化碳,利用C装置吸收二氧化碳;分液漏斗中如果用盐酸代替硫酸,盐酸易挥发,这样制得二氧化碳气体中含氯化氢,浓硫酸不能吸收氯化氢,则氯化氢被碱石灰吸收,导致测到二氧化碳质量偏高,
(2)结合反应定量关系和元素守恒计算得到物质的质量,来计算物质含量;
(3)二氧化碳气体不能全部进入C装置被吸收,需要添加一个装置二氧化碳气体赶入装置C的装置。
[方案一](1)碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,反应方程式为:2NaHCO3![]() Na2CO3+H2O+CO2↑,
Na2CO3+H2O+CO2↑,
因此,本题正确答案是:2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
(2)实验原理是根据加热前后固体质量变化来计算碳酸氢钠,故应保证碳酸氢钠完全分解,加热恒重则碳酸氢钠完全分解,
因此,本题正确答案是:保证NaHCO3分解完全;
[方案二](1)过滤时需用玻璃棒引流,
因此,本题正确答案是:玻璃棒;
(2)可取上层清液,继续加沉淀剂,看是否生成沉淀,具体操作为:取上层清液少许于试管中,加入氢氧化钡溶液,若无沉淀生成,则沉淀完全,
因此,本题正确答案是:取少量上层清液于试管中,滴加一滴Ba(OH)2溶液,观察是否有白色沉淀生成;
[方案三]
(1)B中为浓硫酸吸收水,干燥二氧化碳;分液漏斗中如果用盐酸代替硫酸,盐酸易挥发,这样制得二氧化碳气体中含氯化氢,浓硫酸不能吸收氯化氢,则氯化氢被碱石灰吸收,导致测到二氧化碳质量偏高,等质量碳酸钠和碳酸氢钠,碳酸氢钠产生二氧化碳多,则会导致碳酸氢钠偏多,碳酸钠偏小,
因此,本题正确答案是:浓硫酸;不能;
(2)设Na2CO3和NaHCO3的物质的量分别为x、y,则
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
1 1
x x
2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑
2 2
y
106x+84y=17.90
44x+44y=8.80
联立方程组,解得x=0.05mol,y=0.15mol
则样品中NaHCO3的质量分数为![]() ×100%=70.4%,
×100%=70.4%,
因此,本题正确答案是:70.4%;
(3)实验装置还存在一个明显缺陷为装置中的二氧化碳不能被C全部吸收,则需设计一个装置将A、B中的CO2全部吹入C中吸收,
因此,本题正确答案是:缺少一套将A、B装置内的CO2气体驱赶到C装置中的装置。

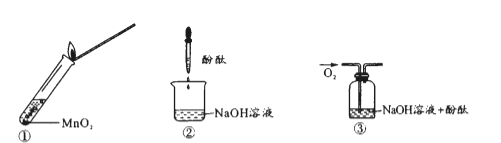
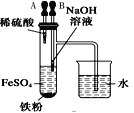
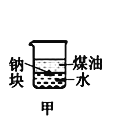
【题目】下列装置所示的实验中,不能达到实验目的是
|
|
|
|
A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)< ρ(钠) < ρ(水) | C.探究氧化性: KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3的热稳定性 |
A. A B. B C. C D. D