题目内容
下列各组物质充分反应后的产物中,滴入KSCN溶液显红色的是( )
| A、FeO和稀盐酸 |
| B、过量铁粉跟稀硫酸 |
| C、氯水跟FeCl2溶液 |
| D、过量铁粉跟硫酸铁溶液 |
考点:二价Fe离子和三价Fe离子的检验
专题:元素及其化合物
分析:各组物质充分反应后的产物中,滴入KSCN溶液显红色,说明反应后溶液中有Fe3+,铁离子与硫氰根离子发生了反应:Fe3++3SCN-?Fe(SCN)3,溶液显示红色,据此进行判断.
解答:
解:A.FeO与稀盐酸反应的离子方程式为:FeO+2H+=Fe2++H2O,反应生成的是Fe2+,滴入硫氰化钾后溶液不显示红色,故A错误;
B.过量铁粉跟稀硫酸反应生成亚铁离子:Fe+2H+=Fe2++H2↑,反应生成的是Fe2+,滴入硫氰化钾后溶液不显示红色,故B错误;
C.氯水跟FeCl2溶液反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,反应生成了铁离子,滴入硫氰化钾后溶液发生了反应:Fe3++3SCN-?Fe(SCN)3,溶液显示红色,故C正确;
D.过量铁粉跟硫酸铁溶液反应的离子方程式为:2Fe3++Fe=3Fe2+,反应生成的是Fe2+,滴入硫氰化钾后溶液不显示红色,故D错误;
关系C.
B.过量铁粉跟稀硫酸反应生成亚铁离子:Fe+2H+=Fe2++H2↑,反应生成的是Fe2+,滴入硫氰化钾后溶液不显示红色,故B错误;
C.氯水跟FeCl2溶液反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,反应生成了铁离子,滴入硫氰化钾后溶液发生了反应:Fe3++3SCN-?Fe(SCN)3,溶液显示红色,故C正确;
D.过量铁粉跟硫酸铁溶液反应的离子方程式为:2Fe3++Fe=3Fe2+,反应生成的是Fe2+,滴入硫氰化钾后溶液不显示红色,故D错误;
关系C.
点评:本题考查了铁离子、亚铁离子的检验方法,题目难度不大,注意掌握铁离子、亚铁离子的检验方法,试题有利于提高学生灵活应用所学知识解决实际问题的能力.

练习册系列答案
相关题目
下列气体能使酸性高锰酸钾溶液褪色但又难溶于水,又可用分液漏斗及烧瓶(或广口瓶)不加热装置制取的是( )
| A、H2 |
| B、SO2 |
| C、CH2=CH2 |
| D、CH≡CH |
关于制备氢氧化铁胶体的正确操作方法( )
| A、在氯化铁溶液中滴入氢氧化钠溶液 |
| B、加热煮沸氯化铁溶液 |
| C、把氯化铁溶液滴入热水中 |
| D、把饱和的氯化铁溶液滴入到沸水中 |
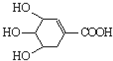 国家卫生和计生委通报:截止4月21日,H7N9禽流感在我国已发现并确诊96例患者.八角茴香含有一种抗亚洲禽流感病毒的重要成分--莽草酸,其分子结构如图.下列关于莽草酸的说法错误的是( )
国家卫生和计生委通报:截止4月21日,H7N9禽流感在我国已发现并确诊96例患者.八角茴香含有一种抗亚洲禽流感病毒的重要成分--莽草酸,其分子结构如图.下列关于莽草酸的说法错误的是( )| A、遇FeCl3溶液呈紫色 |
| B、分子式为C7H10O5 |
| C、能使溴水褪色 |
| D、能溶于水 |
恒温下,容积均为2L的密闭容器M、N中,分别有以下列两种起始投料建立的可逆反应3A(g)+2B(g)?2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3mol A、2mol B;2min达平衡,生成D 1.2mol,测得从反应开始到平衡C的速率为0.3mol?(L?min)-1.N:2mol C、y mol D;达平衡时c(A)=0.6mol?L-1.下列推断的结论中不正确的是( )
| A、x=2 |
| B、平衡时M中c(A)>0.6 mol/L |
| C、y≥2 |
| D、M、N达到平衡时容器中各物质浓度相等 |
下列叙述正确的是( )
| A、水呈液态、氯化氢在同族元素的氢化物中熔沸点最低可用同一原理解释 |
| B、工业上通常用电解Na、Fe、Cu对应的氯化物制得该三种金属单质 |
| C、S、Cl都有较强的非金属性,S,Cl2都可以将Fe氧化为+3价 |
| D、Al(OH)3、Cu(OH)2均不能在氨水中溶解 |
下列有关物质提纯的方法正确的是( )
| 选项 | 待提纯物质 | 杂质 | 主要操作方法 |
| A | 溴苯 | 苯 | 加入铁粉和溴,过滤 |
| B | 碘水 | 水 | 用酒精萃取碘水中的碘 |
| C | 乙烷 | 乙烯 | 通入酸性高锰酸钾溶液,洗气 |
| D | 碘化钾 | 淀粉 | 多次渗析 |
| A、A | B、B | C、C | D、D |
下列叙述错误的是( )
| A、使阴、阳离子结合成化合物的静电作用叫做离子键 |
| B、含共价键的化合物不一定是共价化合物 |
| C、化合物中只要含有离子键就一定属于离子化合物 |
| D、金属元素与非金属元素相化合时一定形成离子键 |
下列除杂(括号内为杂质)实验设计能达到预期目的是( )
| A、乙烷(乙烯):KMnO4酸性溶液,洗气 |
| B、乙醇(乙酸):碱石灰,蒸馏 |
| C、甲苯(苯酚):浓溴水,过滤 |
| D、溴乙烷(乙醇):苯,分液 |