��Ŀ����
�����£��ݻ���Ϊ2L���ܱ�����M��N�У��ֱ���������������ʼͶ�Ͻ����Ŀ��淴Ӧ3A��g��+2B��g��?2C��g��+xD��s���Ļ�ѧƽ��״̬������������£�M��3mol A��2mol B��2min��ƽ�⣬����D 1.2mol����ôӷ�Ӧ��ʼ��ƽ��C������Ϊ0.3mol?��L?min��-1��N��2mol C��y mol D����ƽ��ʱc��A��=0.6mol?L-1�������ƶϵĽ����в���ȷ���ǣ�������
| A��x=2 |
| B��ƽ��ʱM��c��A����0.6 mol/L |
| C��y��2 |
| D��M��N�ﵽƽ��ʱ�����и�����Ũ����� |
���㣺��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
������A������C�����ʼ�������C�����ʵ��������������ʵ���֮�ȵ��ڻ�ѧ������֮�ȼ���x��ֵ��
B������C�����ʼ����c��C��������Ũ�ȱ仯��֮�ȵ��ڻ�ѧ������֮�ȼ����c��A����A��ƽ��Ũ��=A��ʼŨ��-��c��A����
C����B�м����֪M��A��ƽ��Ũ�ȣ��ж�M��N�Ƿ��ǵ�Чƽ�⣬��Ϊ��Чƽ�⣬��ѧ������ת�����������n��A��=3mol��n��B��=2mol�����������ƽ�⣬������ƽ�ⳣ�����㣻
D����B�м����֪A��ƽ��Ũ�ȣ�����M�е�A��ƽ��Ũ�ȷ����жϣ�
B������C�����ʼ����c��C��������Ũ�ȱ仯��֮�ȵ��ڻ�ѧ������֮�ȼ����c��A����A��ƽ��Ũ��=A��ʼŨ��-��c��A����
C����B�м����֪M��A��ƽ��Ũ�ȣ��ж�M��N�Ƿ��ǵ�Чƽ�⣬��Ϊ��Чƽ�⣬��ѧ������ת�����������n��A��=3mol��n��B��=2mol�����������ƽ�⣬������ƽ�ⳣ�����㣻
D����B�м����֪A��ƽ��Ũ�ȣ�����M�е�A��ƽ��Ũ�ȷ����жϣ�
���
�⣺A���ӷ�Ӧ��ʼ��ƽ�⣬C������Ϊ0.3mol��L?min�������n��C��=0.3mol��L?min����2min��2L=1.2mol�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ�����2��x=1.2mol��1.2mol�����x=2����A��ȷ��
B���ӷ�Ӧ��ʼ��ƽ�⣬C������Ϊ0.3mol��L?min�������ԡ�c��C��=0.3mol��L?min����2min=0.6mol/L��Ũ�ȱ仯��֮�ȵ��ڻ�ѧ������֮�ȣ����ԡ�c��A��=
��c��C��=
��0.6mol/L=0.9mol/L������ƽ��ʱc��A��=
-0.9mol/L=0.6mol/L����B����
C����B�м����֪M��A��ƽ��Ũ��Ϊ0.6mol/L������M��N�ǵ�Чƽ�⣬��ѧ������ת�����������n��A��=3mol��n��B��=2mol��ǡ��ת��ʱy=3mol��
=2mol������DΪ���壬��y��2����C��ȷ��
D��B���������֪��M�����У�ƽ��ʱc��A��=
-0.9mol/L=0.6mol/L��N�����м���2molC��2molD��M�����дﵽ��ͬ��ƽ��״̬�����Ը�����Ũ����ͬ����D��ȷ��
��ѡB��
B���ӷ�Ӧ��ʼ��ƽ�⣬C������Ϊ0.3mol��L?min�������ԡ�c��C��=0.3mol��L?min����2min=0.6mol/L��Ũ�ȱ仯��֮�ȵ��ڻ�ѧ������֮�ȣ����ԡ�c��A��=
| 3 |
| 2 |
| 3 |
| 2 |
| 3mol |
| 2L |
C����B�м����֪M��A��ƽ��Ũ��Ϊ0.6mol/L������M��N�ǵ�Чƽ�⣬��ѧ������ת�����������n��A��=3mol��n��B��=2mol��ǡ��ת��ʱy=3mol��
| 2 |
| 3 |
D��B���������֪��M�����У�ƽ��ʱc��A��=
| 3mol |
| 2L |
��ѡB��
���������⿼�黯ѧƽ����㡢��ѧ��Ӧ���ʼ��㣬�Ѷ��еȣ�ע�����õ�Чƽ����Ҳ��������ƽ�ⳣ�����н��

��ϰ��ϵ�д�
 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
�����Ŀ
���и������ʵ�ȼ������ȵ��ǣ�������
| A��̼�Ͷ�����̼ |
| B��1mol̼��3mol̼ |
| C��3mol��Ȳ��C2H2����1mol�� |
| D�����ۺ���ά�� |
�л���Ӧ�����ͺܶ࣬���и���Ӧ����CH2�TCH2��CH2Br-CH2Br�ı仯����ͬһ��Ӧ���͵��ǣ�������
| A��C2H5Cl��CH2�TCH2 |
| B��CH3CHO��C2H5OH |
C��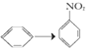 |
| D��CH3COOH��CH3COOC2H5 |
ϩ����CO�� H2��ij�ִ��������·�����Ӧ����ȩ���磺RCH=CH2+CO+H2
RCH2CH2CHO��RCH��CH3��CHO�����ַ�Ӧ��Ϊ�ʻ��ϳɷ�Ӧ��Ҳ����ϩ����ȩ����Ӧ�����ж��ɷ���ʽΪC4H8��ϩ������̼���ϳɷ�Ӧ�õ����л����ﹲ�У�������
| ���� |
| A��3�� | B��4�� | C��5�� | D��6�� |
����ɫ������Һ���ܴ���������ǣ�������
| A��HCO3-��Na+��OH-��Cl- |
| B��Ca2+��NO3-��SO42-��CO32- |
| C��Fe2+��Na+��H+��NO3- |
| D��Cl-��Mg2+��Na+��SO42- |
���и������ʳ�ַ�Ӧ��IJ����У�����KSCN��Һ�Ժ�ɫ���ǣ�������
| A��FeO��ϡ���� |
| B���������۸�ϡ���� |
| C����ˮ��FeCl2��Һ |
| D���������۸���������Һ |
��6molA�����5molB�����Ϸ���4L�ܱ������У���һ�������·�����Ӧ��3A��g��+B��g��?2C��g��+xD��g������5min�ﵽƽ�⣬��ʱ����CΪ2mol���ⶨD��ƽ����Ӧ����Ϊ0.1mol/��L?min��������˵��������ǣ�������
| A��x=2 |
| B��B��ת����Ϊ20% |
| C��ƽ��ʱA��Ũ��Ϊ0.8mol/L |
| D�����´�ƽ��ʱ�����ڵ�ѹǿ�뿪ʼʱ��� |
�����й�������Ӧʵ���˵����ȷ���ǣ�������
| A���Թ�Ҫ��Ũ���������ˮϴ�� |
| B������ˮԡ���ȣ�����ֱ�Ӽ��� |
| C����2%��ϡ��ˮ�е���2%����������Һ�����������Һ |
| D������Ũ����ϴȥ���� |
���з�Ӧ�У�ˮ�Ȳ�����������Ҳ���ǻ�ԭ��������Ӧ��������ԭ��Ӧ���ǣ�������
| A��2Na2O2+2H2O�T4NaOH+O2�� | ||||
B��C+H2O
| ||||
| C��CO2+NH3+H2O�TNH4HCO3 | ||||
| D��2F2+2H2O�T4HF+O2 |