题目内容
下列叙述错误的是( )
| A、使阴、阳离子结合成化合物的静电作用叫做离子键 |
| B、含共价键的化合物不一定是共价化合物 |
| C、化合物中只要含有离子键就一定属于离子化合物 |
| D、金属元素与非金属元素相化合时一定形成离子键 |
考点:离子键的形成,离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:A.离子键指带相反电荷离子之间的相互作用;
B.离子化合物中也可能含共价键,如氢氧化钠;
C.离子化合物中一定含有离子键,可能含有共价键;共价化合物中只含共价键;
D.金属元素和非金属元素化合不一定形成离子键;
B.离子化合物中也可能含共价键,如氢氧化钠;
C.离子化合物中一定含有离子键,可能含有共价键;共价化合物中只含共价键;
D.金属元素和非金属元素化合不一定形成离子键;
解答:
解:A.使阴、阳离子结合成化合物的静电作用叫做离子键,故A正确;
B.含共价键的化合物不一定是共价化合物,如氢氧化钠中含有共价键,但属于离子化合物,故B正确;
C.化合物中只要含有离子键就肯定属于离子化合物,故C正确;
D.金属元素和非金属元素化合不一定形成离子键,可能形成共价键,如氯化铝中只含共价键,故D错误;
故选D.
B.含共价键的化合物不一定是共价化合物,如氢氧化钠中含有共价键,但属于离子化合物,故B正确;
C.化合物中只要含有离子键就肯定属于离子化合物,故C正确;
D.金属元素和非金属元素化合不一定形成离子键,可能形成共价键,如氯化铝中只含共价键,故D错误;
故选D.
点评:本题考查了离子键的判断,根据物质的构成微粒、微粒间的作用力结合离子键的概念来分析解答,难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
气体甲通入溶液乙中时,随着甲的通入,溶液乙的颜色逐渐褪去,下列说法正确的是( )
| A、气体甲一定具有漂白性 |
| B、溶液乙褪色后,不可能再恢复原来的颜色 |
| C、气体甲一定与溶液乙中的某种有色物质发生化合反应 |
| D、气体甲可能被溶液乙中的某些离子氧化 |
下列各组物质充分反应后的产物中,滴入KSCN溶液显红色的是( )
| A、FeO和稀盐酸 |
| B、过量铁粉跟稀硫酸 |
| C、氯水跟FeCl2溶液 |
| D、过量铁粉跟硫酸铁溶液 |
归纳与推理是化学学习常用的方法.下列推理正确的是( )
| A、因为稀硫酸能与铁反应放出H2,所以稀硝酸与铁反应也一定能放出H2 |
| B、同族元素具有相似性.因为CaCO3、BaCO3是白色沉淀,所以SrCO3也是白色沉淀 |
| C、蔗糖加入浓硫酸后变黑,说明浓硫酸具有吸水性 |
| D、因为SO2可以使酸性KMnO4溶液褪色,所以SO2具有漂白性 |
下列有关银镜反应实验的说法正确的是( )
| A、试管要用浓硫酸和蒸馏水洗涤 |
| B、采用水浴加热,不能直接加热 |
| C、向2%的稀氨水中滴入2%的硝酸银溶液,配得银氨溶液 |
| D、可用浓盐酸洗去银镜 |
1mol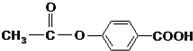 在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )
在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )
 在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )
在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )| A、2mol | B、3mol |
| C、4mol | D、5mol |
可逆反应:2HI(g)?H2(g)+I2(g);△H>0.在密闭容器中进行,当达到平衡时欲使混合气体的颜色加深,应采取的措施( )
| A、增大容器体积 |
| B、降低温度 |
| C、加入催化剂 |
| D、充入I2气体 |
下列各组离子中,能在溶液中大量共存的是( )
| A、Na+ H+ NO3- Fe2+ |
| B、Ca2+ NO3- HCO3- OH- |
| C、K+ H+ Cl- SO42- |
| D、Fe3+ Cl- H+ CO32- |