题目内容
已知在Na2SO4、K2SO4、MgCl2的混合液中,c(Na+)=0.1mol/L,c(K+)=0.2mol/L,c(Cl-)=0.4mol/L,c(SO42-)=0.1mol/L,则c(Mg2+)为 .
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:根据溶液中阴阳离子所带的正负电荷总数相等,则有c(Na+)+c(K+)+2c(Mg2+)=c(Cl-)+2c(SO42-),据此计算.
解答:
解:根据溶液中阴阳离子所带的正负电荷总数相等,则有c(Na+)+c(K+)+2c(Mg2+)=c(Cl-)+2c(SO42-),即:0.1mol/L×1+0.2mol/L×1+2c(Mg2+)=0.4mol/L×1+0.1mol/L×2,
解得:c(Mg2+)=0.15mol/L,
故答案为:0.15mol/L.
解得:c(Mg2+)=0.15mol/L,
故答案为:0.15mol/L.
点评:本题考查物质的量浓度的有关计算,明确溶液不显电性是解答本题的关键,难度不大.

练习册系列答案
相关题目
重铬酸钾溶液中存在如下平衡:Cr2O72-(橙红色)+H2O?2H++2CrO42-(黄色),向K2Cr2O7溶液中加入下列哪种试剂,溶液颜色会从黄色逐渐变为橙红色( )
| A、NaHSO4 |
| B、NaHCO3 |
| C、Na2CO3 |
| D、CH3COONa |
 50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: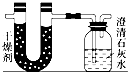 已知某醇燃料含有碳、氢、氧三种元素.为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如下表所列的实验结果(假设产生的气体完全被吸收):
已知某醇燃料含有碳、氢、氧三种元素.为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如下表所列的实验结果(假设产生的气体完全被吸收):