题目内容
13.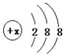 有几种元素的微粒电子层结构如图所示,其中:
有几种元素的微粒电子层结构如图所示,其中:(1)某电中性微粒一般不和其他元素的原子反应,这种微粒符号是Ar;
(2)盐溶液中的某微粒与AgNO3溶液反应时会出现白色浑浊,这种微粒符号是Cl-,生成该白色浑浊的离子方程式为Cl-+Ag+=AgCl↓;
(3)某微粒具有还原性,且这种微粒失去2个电子即变为原子,这种微粒的符号是S 2-,该微粒的电子式为:
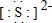 .
.
分析 (1)该微粒属于电中性粒子,则质子数等于核外电子数=2+8+8=18,元素质子数等于原子序数;
(2)盐溶液中的某微粒与AgNO3溶液反应时会出现白色浑浊,则该微粒是氯离子,氯离子和银离子反应生成AgCl白色沉淀;
(3)某微粒具有还原性,且这种微粒失去2个电子即变为原子,且离子核外电子数是18,则该微粒质子数=18-2=16,为硫离子.
解答 解:(1)该微粒属于电中性粒子,则质子数等于核外电子数=2+8+8=18,元素质子数等于原子序数,所以该微粒为Ar,故答案为:Ar;
(2)盐溶液中的某微粒与AgNO3溶液反应时会出现白色浑浊,且离子核外有18个电子,则该微粒是Cl-,氯离子和银离子反应生成AgCl白色沉淀,离子方程式为Cl-+Ag+=AgCl↓,
故答案为:Cl-;Cl-+Ag+=AgCl↓;
(3)某微粒具有还原性,且这种微粒失去2个电子即变为原子,且离子核外电子数是18,则该微粒质子数=18-2=16,为S 2-,电子式为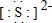 ,故答案为:S 2-;
,故答案为:S 2-;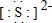 .
.
点评 本题考查离子方程式的书写、原子结构示意图、电子式等知识点,明确电子式、质子数与电荷关系即可解答,注意硫离子书写特点,为易错点.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
19.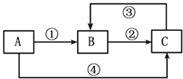 A、B、C三种物质中均含有同一种元素M,它们之间有如下图所示的转化关系(部分反应物质已略去).A为一种金属单质,反应①②③均为化合反应,反应④为置换反应.下列有关说法不正确的是( )
A、B、C三种物质中均含有同一种元素M,它们之间有如下图所示的转化关系(部分反应物质已略去).A为一种金属单质,反应①②③均为化合反应,反应④为置换反应.下列有关说法不正确的是( )
 A、B、C三种物质中均含有同一种元素M,它们之间有如下图所示的转化关系(部分反应物质已略去).A为一种金属单质,反应①②③均为化合反应,反应④为置换反应.下列有关说法不正确的是( )
A、B、C三种物质中均含有同一种元素M,它们之间有如下图所示的转化关系(部分反应物质已略去).A为一种金属单质,反应①②③均为化合反应,反应④为置换反应.下列有关说法不正确的是( )| A. | ①中所加试剂可能是氯气 | |
| B. | ③中需要加具有氧化性的试剂 | |
| C. | A与稀硝酸反应一定能实现元素M在①中发生的价态变化 | |
| D. | 元素M在②中发生的价态变化也能通过加碘化钾溶液实现 |
1.元素A的单质及A与B形成的化合物能按如图所示的关系发生转化.则下列说法正确的是( )
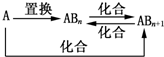

| A. | 图中物质间的转化都不是氧化还原反应 | |
| B. | 当n=1时,A可能是N2 | |
| C. | A一定是金属元素 | |
| D. | 当n=2时,A可能是Fe |
18.已知反应:
①101KPa时,2C(s)+O2(g)=2CO(g);△H=-221KJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3KJ/mol
下列结论正确的是( )
①101KPa时,2C(s)+O2(g)=2CO(g);△H=-221KJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3KJ/mol
下列结论正确的是( )
| A. | 碳的燃烧热等于110.5KJ/mol | |
| B. | 2C(s)+2O2(g)=2CO2(g);△H>-221 KJ/mol | |
| C. | 浓硫酸与稀NaOH溶液反应的中和热为-57.3 KJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出热量小于57.3 KJ |
5.在 Na2CO3溶液中,下列离子浓度关系正确的是( )
| A. | c(Na+)>c(CO32-)>c(H+)>c(OH-) | B. | c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) | ||
| C. | c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) | D. | c(H+)+c(HCO3-)+2 c(H2CO3)=c(OH-) |
2.一定温度下,反应N2(g)+3H2(g)?2NH3(g)达到化学平衡状态的标志( )
| A. | N2、H2和NH3的质量分数不再改变 | |
| B. | c(N2):c(H2):c(NH3)=1:3:2 | |
| C. | N2与H2的物质的量之和是NH3的物质的量2 | |
| D. | 单位时间里每增加1 mol N2,同时增加3 mol H2 |
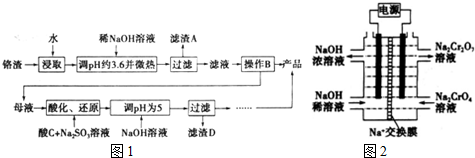
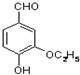 是食品添加剂的增香原料,其香味比香草醛更浓郁.
是食品添加剂的增香原料,其香味比香草醛更浓郁.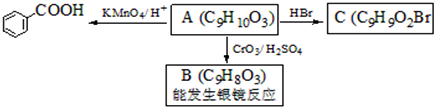
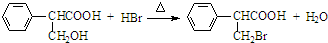 ,属于取代反应(填反应类型).
,属于取代反应(填反应类型). .
. .
.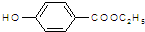 )是一种医药中间体,请设计合理方案用
)是一种医药中间体,请设计合理方案用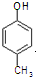 合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).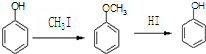

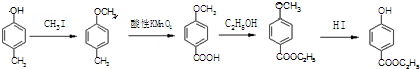
 .
.