��Ŀ����
����Ŀ������˵����ȷ���ǣ�������
A.��KClO3���KCl������뻹ԭ��
B.�������Һ�м�����������������Һ�������кͷ�Ӧ����Һ�ĵ�����������
C.��֪��ˮ���ܶȱ�ˮС����Ũ��Խ���ܶ�ԽС�������������ֱ�Ϊ5%��15%�İ�ˮ�������ϣ��õ�����Һ��������������10%
D.һ�������£�H2��O2�Ļ������Ե���������ܶ�Ϊ1����H2��O2�����ʵ���֮��Ϊ2��13
���𰸡�D
��������A��KClO3���ȷֽ���Ա��KCl�����Բ�һ��Ҫ���뻹ԭ����A���������⣻
B��������������ʣ���ˮ��Һ�в��ֵ��룬������������������Һ�����߷�Ӧ����ǿ����ʴ����ƣ���Һ������Ũ��������Һ��������ǿ��B���������⣻
C����ˮŨ��Խ���ܶ�ԽС�����������ʱ��Ũ�Ƚ�ϡ�İ�ˮ�����ϴ���Ũ�İ�ˮ��������С��������Ϻ������������ӽ�ϡ��ˮ��Ũ�ȣ�������ҺŨ�ȵ�ȻҪ��ԭ����������������ƽ��ֵƫСЩ����С��10%��C���������⣻
D��H2��O2�Ļ�����壬���ܶ�����ͬ�����µ�����1������M=28��1=28g/mol�������ʵ����ֱ�Ϊx��y���� ![]() =28�����x��y=2��13��D�������⣻
=28�����x��y=2��13��D�������⣻
���Դ��ǣ�D��

 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д�����Ŀ��һ�������£�ͨ�����з�Ӧ�����Ʊ������մɵ�ԭ��MgO��
MgSO4��s��+CO��g��MgO��s��+CO2��g��+SO2��g����H��0
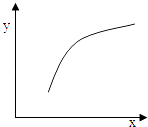
�÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ�к�����x��ֵ�����´ﵽƽ���������y��x�仯���ƺ������ǣ� ��
ѡ�� | x | y |
A | �¶� | �����ڻ��������ܶ� |
B | CO�����ʵ��� | CO2��CO�����ʵ���֮�� |
C | SO2��Ũ�� | ƽ�ⳣ��K |
D | MgSO4����������������� | CO��ת���� |
A.A
B.B
C.C
D.D
