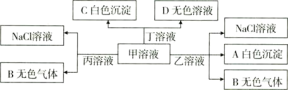
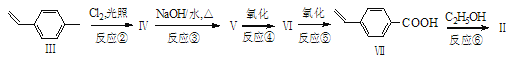题目内容
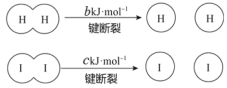
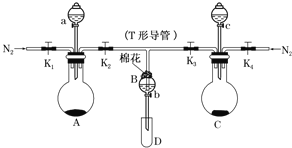
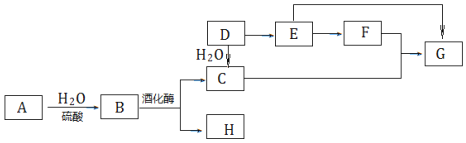
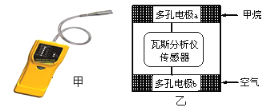
【题目】有一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷达到一定浓度时,通过传感器显示出来,其装置如图乙所示,ab间充有固体电解质Y2O3-Na2O,允许O2-自由移动。下列叙述正确的是
A.瓦斯分析仪工作时,电池内电路中, O2-由电极a流向电极b
B.电池外电路中电子由正极流向负极
C.电极a的反应式为:CH4+4O2--8e-=CO2+2H2O
D.当固体电解质中有1 mol O2-通过时,电子转移4 mol
【答案】C
【解析】
该装置是燃料电池,通入甲烷的电极a是负极、通入空气的电极b是正极,放电时,负极反应式为CH4+4O2--8e-═CO2+2H2O,正极反应式为O2+4e-=2O2-,电子从负极沿导线流向正极,原电池内部阳离子向正极移动、阴离子向负极移动,据此分析解答。
A. 该原电池中,正极上氧气得电子发生还原反应,所以通入空气的电极b是正极,内电路中阴离子向负极移动,所以O2由电极b流向电极a,故A错误;
B. 电池外电路中电子从负极沿导线流向正极,故B错误;
C. a是负极,负极上甲烷失电子和氧离子反应生成二氧化碳和水:CH4+4O2--8e-=CO2+2H2O,故C正确;
D. 每个O原子得到2个电子生成O2,所以当固体电解质中有1molO2通过时,电子转移2mol,故D错误;
答案选C。

练习册系列答案
相关题目