题目内容
【题目】某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略)。
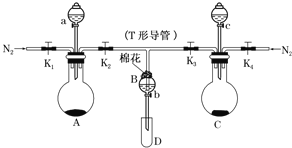
(1)按图连接好装置,检查A装置的气密性的方法为___。
(2)检查完装置的气密性,添加药品,向A装置的分液漏斗中加入浓盐酸,在圆底烧瓶中加入固体KMnO4;向B装置中加入10mLFeCl2溶液;在C装置的分液漏斗中加入70%的硫酸,向圆底烧瓶中加入固体Na2SO3;棉花浸润___溶液。打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2,然后关闭K1,K3,K4。通入一段时间N2的目的是___。
(3)打开活塞a,逐滴加入浓盐酸,当B中溶液变为棕黄色时,停止滴加浓盐酸,夹紧K2,打开活塞b,使约2mL的溶液流入D试管中,分别取1mL溶液滴入___(填试剂名称)和铁氰化钾溶液可以证明其中含有Fe3+和Fe2+。A装置中发生反应的离子方程式为___。
(4)打开K3和活塞c,逐滴加入70%的硫酸,当B中溶液颜色逐渐变为___色,停止滴加70%的硫酸,夹紧K3,打开活塞b,使约2mL的溶液流入D试管中,并检验其中的离子。B中发生反应的离子方程式为___。
(5)结合实验现象判断Fe3+、Cl2、SO2氧化性由弱到强的顺序为___。
【答案】关闭a、b、K1、K3,打开K2,向B装置中加水,将T形导管下端插入水中,微热A装置,看到有气泡产生,停止加热恢复室温,T形导管下端形成一段水柱,说明A装置气密性良好 NaOH 排出装置中的空气,防止其干扰实验 硫氰化钾 2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O 浅绿 SO2+2Fe3++2H2O=2Fe2++SO42-+4H+ SO2<Fe3+<Cl2
【解析】
(1)检查装置气密性,首先要密闭,应关闭a、b、K1、K3,打开K2,向B装置中加水,T形导管下端插入水中,微热A装置,看到有气泡产生,停止加热恢复室温,T形导管下端形成一段水柱,说明A装置气密性良好;
(2)用碱溶液为尾气处理装置;通入一段时间N2的目的是排出装置中的空气;
(3)Fe3+遇KSCN溶液变为血红色;A装置中酸性条件下高锰酸根离子将氯离子氧化成氯气;
(4)Fe3+被SO2还原为Fe2+;B中二氧化硫被铁离子氧化成硫酸;
(5)根据方程式,氧化剂的氧化性大于氧化产物。
(1)检查装置气密性,首先要密闭,应关闭a、b、K1、K3,打开K2,向B装置中加水,T形导管下端插入水中,微热A装置,看到有气泡产生,停止加热恢复室温,T形导管下端形成一段水柱,说明A装置气密性良好;
(2)用碱溶液吸收多余的氯气、二氧化硫,防止污染空气;通入一段时间N2的目的是排出装置中的空气,防止其干扰实验;
(3)氯气将氯化亚铁中的Fe2+氧化为Fe3+,Fe3+遇KSCN溶液变为血红色,则用硫氰化钾可以证明其中含有Fe3+;A装置中酸性条件下高锰酸根离子将氯离子氧化成氯气,反应的离子方程式为:2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O;
(4)Fe3+被SO2还原为Fe2+,溶液变为浅绿色;B中二氧化硫被铁离子氧化成硫酸,反应的离子方程式为:SO2+2Fe3++2H2O=2Fe2++SO42-+4H+;
(5)结合实验现象及氧化还原反应原理可知:Cl2、Fe3+和SO2的氧化性由弱到强的顺序为:SO2<Fe3+<Cl2。