题目内容
14.下列各组稀溶液中,利用组内物质的相互反应,就能将各种物质鉴别的是( )| A. | NaOH、CuSO4、HCl、KNO3 | B. | HCl、KOH、NaCl、Na2SO4 | ||
| C. | Ca(OH)2、Na2CO3、NaCl、HCl | D. | NaNO3、MgCl2、KCl、Ba(OH)2 |
分析 如果物质之间混合时现象不同,如生成气体、沉淀、有颜色变化等,则可以鉴别,否则无法鉴别,据此分析解答.
解答 解:A.硫酸铜溶液呈蓝色,硫酸铜和NaOH溶液反应生成蓝色沉淀,和HCl、KNO3都不反应而导致现象相同,无法鉴别,故A错误;
B.这几种物质相互混合时都没有明显现象变化,所以不能鉴别,故B错误;
C.Ca(OH)2、Na2CO3混合产生白色沉淀,Na2CO3、HCl混合生成无色气体,NaCl和其余三种物质混合无明显现象,所以现象不同,可以鉴别,故C正确;
D.MgCl2、Ba(OH)2反应生成白色沉淀,但MgCl2、Ba(OH)2分别和NaNO3、KCl混合时都无明显现象,所以无法鉴别,故D错误;
故选C.
点评 本题考查物质鉴别和检验试验方案设计,为高频考点,明确元素化合物性质是解本题关键,利用物质之间反应的差异性分析解答,题目难度不大.

练习册系列答案
相关题目
4.下列表示对应化学反应的离子方程式正确的是( )
| A. | 次氯酸钠溶液中加入双氧水有氧气放出:ClO-+H2O2═O2↑+Cl-+H2O | |
| B. | 碳酸钙溶于稀醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 用稀硝酸洗涤做过银镜反应的试管:Ag+4H++NO3-═Ag++NO↑+2H2O | |
| D. | 苯酚钠溶液中通入少量CO2: |
2.某学习小组探究金属与不同酸反应的差异,以及影响反应速率的因素.
实验药品:2.0moL/L盐酸、4.0mol/L盐酸、2.0mol/L硫酸、4.0mol/L硫酸,相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50.0mL,金属用量均为9.0g.
(1)帮助该组同学完成以上实验设计表.
(2)该小组同学在对比①和⑤实验时发现①的反应速度都明显比⑤快,你能对问题原因作出哪些假设或猜想(列出一种即可)?Cl-能够促进Al与H+的反应或SO42-对Al与H+的反应起阻碍作用.
实验药品:2.0moL/L盐酸、4.0mol/L盐酸、2.0mol/L硫酸、4.0mol/L硫酸,相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50.0mL,金属用量均为9.0g.
(1)帮助该组同学完成以上实验设计表.
| 实验目的 | 实验编号 | 温度 | 金属铝的形态 | 酸及浓度 |
| 1.实验①和②探究盐酸浓度对该反应速率的影响 2.实验②和③探究探究温度对反应速率的影响 3.实验②和④探究金属规格(铝片,铝粉)对该反应速率的影响 4.①和⑤实验探究铝与稀盐酸和稀硫酸反应的差异 | ① | 25℃ | 铝片 | 4.0moL/L盐酸 |
| ② | 25℃ | 铝片 | 2.0moL/L盐酸 | |
| ③ | 35℃ | 铝片 | 2.0moL/L盐酸 | |
| ④ | 25℃ | 铝粉 | 2.0moL/L盐酸 | |
| ⑤ | 25℃ | 铝片 | 2.0moL/L硫酸 |
9.某结晶水合物的化学式为R•xH2O其相对分子质量为Mr,在25℃时a g晶体溶于b g水中,恰好达饱和,形成V mL溶液,则下列表达式中不正确的是( )
| A. | 饱和溶液的物质的量浓度$\frac{100a(Mr-18x)}{MrV}$ | |
| B. | 饱和溶液的质量分数$\frac{a(Mr-18x)}{(a+b)Mr}$ | |
| C. | 25℃,R的溶解度$\frac{100a(Mr-18x)}{(bMr+18ax)}$ | |
| D. | 饱和溶液的密度$\frac{a+b}{V}$ |
19.为了测定某未知NaOH溶液的浓度,需要0.200mol•L-1的盐酸溶液500mL.某学生用实验室中常用的36.5%(密度为1.20g•cm-3)的浓盐酸配制所需稀盐酸,并设计了以下步骤完成实验.
(1)请你帮助该同学完成以下各步中的内容,并将其所设计的实验步骤正确排序.
A.用b(从以下备选仪器中选取适当仪器将其序号填入)量(或称)取36.5%(密度为1.19g•cm-3)的浓盐酸8.3ml(填写所需体积或质量).
a.50mL量筒; b.10mL量筒; c.托盘天平.
B.将取好的浓盐酸在烧杯中加适量蒸馏水稀释.
C.轻轻振荡后继续加蒸馏水到液面距离仪器刻线1~2cm处.
D.等溶液恢复至室温.
E.将溶液用玻璃棒引流转入500ml容量瓶(填写所需仪器)中,再用适量蒸馏水洗涤烧杯和玻璃棒2~3次一并转入其中.
F.用胶头滴管加蒸馏水直到溶液液面恰好与刻线相切,塞好瓶塞摇匀即可.
以上各实验步骤的正确排列顺序是ABDECF.
(2)准确移取20.00mL待测NaOH溶液于一洁净锥形瓶中,然后用所配标准盐酸溶液进行滴定(以酚酞为指示剂).滴定结果如下表:
根据以上数据计算出未知NaOH溶液的物质的量浓度为0.22mol•L-1(精确到0.01).
(3)下列操作或叙述正确的是BC(填写序号).
A.滴定过程中,眼睛注视滴定管内溶液并使视线与液面的凹面水平.
B.滴定过程中由于摇动锥形瓶使少许溶液溅起沾在瓶内壁,为使测定结果正确,可用少许蒸馏水将其冲入锥形瓶内的溶液中.
C.容量瓶和滴定管在使用前洗净后都要检查是否漏液.
D.向锥形瓶中移取NaOH溶液前,用少许NaOH溶液润洗锥形瓶2~3次.
(4)下列操作或现象会导致测定结果偏高的是ACE(填写序号).
A.滴定过程中不小心将一滴溶液滴在锥形瓶外;
B.滴定结束时,发现在滴定管尖嘴处有小气泡;
C.滴定结束后仰视滴定管液面读数;
D.溶液褪色立即读数,摇动锥形瓶后看到溶液红色复出;
E.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗,直接加入标准液进行滴定.
(1)请你帮助该同学完成以下各步中的内容,并将其所设计的实验步骤正确排序.
A.用b(从以下备选仪器中选取适当仪器将其序号填入)量(或称)取36.5%(密度为1.19g•cm-3)的浓盐酸8.3ml(填写所需体积或质量).
a.50mL量筒; b.10mL量筒; c.托盘天平.
B.将取好的浓盐酸在烧杯中加适量蒸馏水稀释.
C.轻轻振荡后继续加蒸馏水到液面距离仪器刻线1~2cm处.
D.等溶液恢复至室温.
E.将溶液用玻璃棒引流转入500ml容量瓶(填写所需仪器)中,再用适量蒸馏水洗涤烧杯和玻璃棒2~3次一并转入其中.
F.用胶头滴管加蒸馏水直到溶液液面恰好与刻线相切,塞好瓶塞摇匀即可.
以上各实验步骤的正确排列顺序是ABDECF.
| 实验序号 | 滴定管液面起始读数 | 滴定管液面终点读数 |
| 1 | 1.32mL | 23.36mL |
| 2 | 2.26mL | 24.22mL |
根据以上数据计算出未知NaOH溶液的物质的量浓度为0.22mol•L-1(精确到0.01).
(3)下列操作或叙述正确的是BC(填写序号).
A.滴定过程中,眼睛注视滴定管内溶液并使视线与液面的凹面水平.
B.滴定过程中由于摇动锥形瓶使少许溶液溅起沾在瓶内壁,为使测定结果正确,可用少许蒸馏水将其冲入锥形瓶内的溶液中.
C.容量瓶和滴定管在使用前洗净后都要检查是否漏液.
D.向锥形瓶中移取NaOH溶液前,用少许NaOH溶液润洗锥形瓶2~3次.
(4)下列操作或现象会导致测定结果偏高的是ACE(填写序号).
A.滴定过程中不小心将一滴溶液滴在锥形瓶外;
B.滴定结束时,发现在滴定管尖嘴处有小气泡;
C.滴定结束后仰视滴定管液面读数;
D.溶液褪色立即读数,摇动锥形瓶后看到溶液红色复出;
E.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗,直接加入标准液进行滴定.
6.若某原子在处于能量最低状态时,外围电子排布为3d14s2,则下列说法正确的是( )
| A. | 该元素原子处于能量最低状态时,原子中共有3个未成对电子 | |
| B. | 该元素原子核外共有4个能层 | |
| C. | 该元素原子的M能层共有8个电子 | |
| D. | 该元素原子最外层共有3个电子 |
16.某烃的一种同分异构体的一氯代物只有一种,该烃的分子式是( )
| A. | C6H14 | B. | C5H12 | C. | C4H10 | D. | C3H8 |
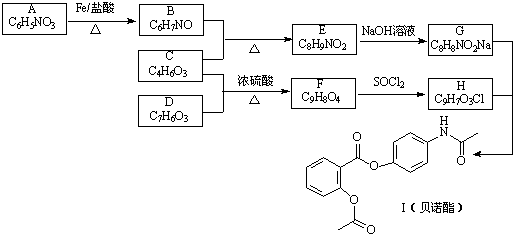
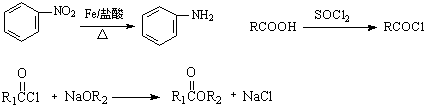
 ,G
,G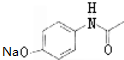 .
. .
. .
. 的合理线路(其他试剂任选,用流程图表示:写出反应物、产物及主要反应条件)
的合理线路(其他试剂任选,用流程图表示:写出反应物、产物及主要反应条件)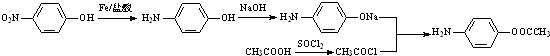 .
.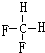 和
和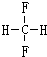
 和CH2=CH-CH2
和CH2=CH-CH2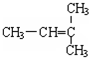 和
和