题目内容
【题目】常温下,![]() ,
,![]() ,
,![]() ,下列说法正确的是
,下列说法正确的是
A. ![]() 与
与![]() 等体积混合后的溶液中:
等体积混合后的溶液中:![]()
B. 用相同浓度的![]() 溶液分别滴定等体积pH均为3的HCOOH和
溶液分别滴定等体积pH均为3的HCOOH和![]() 溶液至终点,消耗
溶液至终点,消耗![]() 溶液的体积相等
溶液的体积相等
C. ![]() 与
与![]() 盐酸等体积混合后的溶液中
盐酸等体积混合后的溶液中![]() :
: ![]()
D. 浓度均为![]() 的
的![]() 和
和![]() 溶液中阳离子的物质的量浓度之和: 前者小于后者
溶液中阳离子的物质的量浓度之和: 前者小于后者
【答案】C
【解析】首先由三种物质的K值可知,HCOOH、CH3COOH、NH3·H2O都是弱电解质,且酸性HCOOH﹥CH3COOH。NH3﹒H2O的电离程度小于HCOOH。A、二者等体积混合反应生成的HCOONa与没有反应的HCOOH物质的量之比为1:1,且HCOOH是一种弱酸,根据电荷守恒的c(H+)+C(Na+)=c(OH-)+c(HCOO-),溶液中的Na+与HCOO(原子团)物质的量之比为1:2,既2c(Na+)=c(HCOO-)+c(HCOOH),代入约去Na+得2c(H+)+ c(HCOOH)=2c(OH-)+2c(HCOO-),A错误。B、因为HCOOH酸性比CH3COOH强,所以HCOOH的电离程度比CH3COOH大, pH值相等的两种溶液中c(H+)相等,所以CH3COOH溶液浓度比HCOOH溶液浓度大,体积相等时,n(CH3COOH) ﹥n(HCOOH),因此CH3COOH中和消耗的NaOH更多,B错误。C、等体积混合后得到的溶液中NaCl、CH3COOH、CH3COONa浓度相等,因为溶液呈酸性,所以CH3COONa的水解可以忽略不计,溶液中由于CH3COOH的部分电离使溶液呈酸性,所以c(Cl-)﹥c(CH3COOH) ﹥c(H+)。c(Cl-)=c(NaCl)=c(CH 3COONa)=c(CH3COO-)1,溶液中c(CH3COO-)等于c(CH3COO-)1加上CH3COOH电离得到的c(CH3COO-)2,所以c(CH3COO-)﹥c(Cl-),C正确。D、0.1mol/L的HCOONa溶液中阳离子的物质的量浓度之和等于c(Na+)+c(H+)1=c(HCOO-)+c(OH-)1,0.1mol/L的NH4Cl溶液中阳离子的物质的量浓度之和等于c(NH4+)+c(H+)2=c(Cl-)+c(OH-)2,且c(Na+)=c(Cl -)。因为NH3·H2O的电离程度小于HCOOH,所以HCOONa水解程度小于NH4Cl,则c(OH-)1<c(H+)2,温度相同时(常温)KW相等,则c(H+)1﹥c(OH-)2,所以c(Na+)+c(H+)1﹥c(Cl-)+c(OH-)2 =c(NH4+)+c(H+)2,所以D错误。正确答案C。

 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案【题目】仔细分析下列实验:
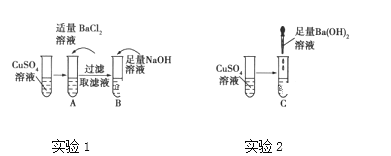
A、B、C试管中的现象如表所示:
试管 | A | B | C |
现象 | 产生白色沉淀, 溶液仍为蓝色 | 产生蓝色沉淀, 溶液变为无色 | 产生蓝色沉淀, 溶液变为无色 |
写出A、B、C试管中所发生反应的离子方程式。
(1)A:______________________________________________。
(2)B:______________________________________________。
(3)C:______________________________________________。