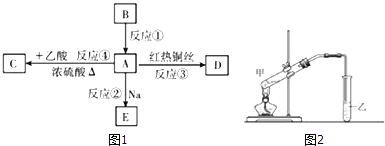
��Ŀ����
����Ŀ��ͭԪ��λ��Ԫ�����ڱ��е���B�壬�ڻ��������仯�ϼۿ��Գ���+1��+2�ۡ�ͭ�ĵ��ʼ��仯�����ںܶ���������Ҫ��Ӧ�á�
��.CuSO4��Cu(NO3)2�dz�����+2��ͭ�Ļ�����н�Ϊ�㷺��Ӧ�á�
��1����CuSO4��Һ�еμӰ�ˮ�������Եõ�����ɫ��[Cu(NH3)4]SO4��Һ��
N��O��S����Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ______________________________��
��2���Ʊ�Cu(NO3)2��һ�ַ�������N2O4������������Һ�м���ͭ����Ӧһ��ʱ����ȼ��ɵõ�Cu(NO3)2��NO3-�����幹�͵�����Ϊ_______________��Nԭ�ӵ��ӻ���ʽΪ________________��NO3-��һ�ֵȵ�����Ϊ________________________��
��.CuCl�ǽ�Ϊ������ʮ1��ͭ�Ļ����
��3����̬Cu+�ļ۲�����Ų�ʽΪ________________________��
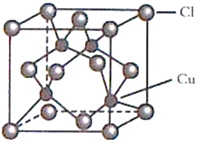
��4��CuCl�ľ����ṹ��ͼ��ʾ��C1ԭ��λ��������Ķ�������ģ� Cuԭ��λ��Clԭ�ӹ��ɵ����������ġ�ÿ��Clԭ����Χ��Clԭ������ҵȾ����Cuԭ����ĿΪ________________��
 ��
��
���𰸡� N��O��S ƽ�������� sp2�ӻ� CO32-��SO3 3d10 4
���������������������ͨ����ͭ�ļ��ֻ�������о�����Ҫ��������ܡ�����ԭ�ӵ��ӻ����ȵ����塢�������ӵ����幹�͡������Ų���������λ����֪ʶ�����鿼�������ʽṹ���֪ʶ��������������鿼����ʵ������ķ���������������ѧ֪ʶ��������������
��������1��N��Oͬ���ڵڶ�������N��2p3��һ�ְ���������ȶ�״̬������N�ĵ�һ�����ܴ���O��O��Sͬ���ڢ�A��Oλ�ڵڶ����ڣ�Sλ�ڵ������ڣ����Ե�һ������O����S����һ������˳��N��O��S����ȷ�𰸣�N��O��S����2��NO3-����ԭ��N��O�γ������ɼ�����Nԭ�ӵŶ���ĿΪ![]() ����������ԭ��N�ļ۲���Ӷ���Ϊ3��N����sp2�ӻ���NO3-����ṹΪƽ�������Ρ��ȵ�������ָ�۵�������ԭ������ͬ�ķ��ӡ���������NO3-�ĵȵ����������CO32-��SO3�ȡ���ȷ�𰸣�ƽ�������Ρ�sp2��CO32-����SO3������3��Cu��29��Ԫ�أ���������Ų�Ϊ[Ar]3d104s1��ʧȥ�����1�������γ�Cu+�����Cu+�ĺ�������Ų�Ϊ[Ar]3d10����̬Cu+�ļ۵����Ų�ʽΪ3d10����ȷ�𰸣�3d10����4������������������һ������ͼ����
����������ԭ��N�ļ۲���Ӷ���Ϊ3��N����sp2�ӻ���NO3-����ṹΪƽ�������Ρ��ȵ�������ָ�۵�������ԭ������ͬ�ķ��ӡ���������NO3-�ĵȵ����������CO32-��SO3�ȡ���ȷ�𰸣�ƽ�������Ρ�sp2��CO32-����SO3������3��Cu��29��Ԫ�أ���������Ų�Ϊ[Ar]3d104s1��ʧȥ�����1�������γ�Cu+�����Cu+�ĺ�������Ų�Ϊ[Ar]3d10����̬Cu+�ļ۵����Ų�ʽΪ3d10����ȷ�𰸣�3d10����4������������������һ������ͼ����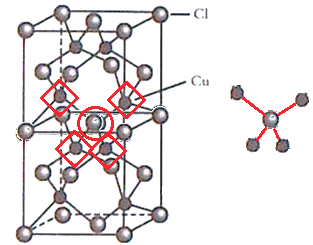 ѡȡ�м��Clԭ����ͼ��Ȧ����Clԭ�ӣ���Ϊ�о������������������Cuԭ�ӷֱ��ǰ�������Clԭ�ӵ�4��Clԭ�ӹ��ɵ����������ĵ�Cuԭ�ӣ���ͼ���α�ǵ�Cuԭ�ӣ������ĸ�Cuԭ��ҲΧ���������壬Clԭ��λ������������������ͼ�ң�����ȷ�𰸣�4��
ѡȡ�м��Clԭ����ͼ��Ȧ����Clԭ�ӣ���Ϊ�о������������������Cuԭ�ӷֱ��ǰ�������Clԭ�ӵ�4��Clԭ�ӹ��ɵ����������ĵ�Cuԭ�ӣ���ͼ���α�ǵ�Cuԭ�ӣ������ĸ�Cuԭ��ҲΧ���������壬Clԭ��λ������������������ͼ�ң�����ȷ�𰸣�4��

����Ŀ��������������Ӱ�����ǵ�����ͽ�����������Ҫ��Ⱦ��Ϊ�����������PM2.5������Ҫ��ԴΪȼú��������β���ȡ���˸�����Դ�ṹ���������ŵȴ�ʩ����Ч����PM2.5��SO2��NOx����Ⱦ��
��ش���������:
(1)��һ������ijPM2.5 ��Ʒ������ˮ�ܽ��Ƴɴ�������(����OH-)�������²�ø���������ɼ���Ũ�����±�:���ݱ��������жϸ�������pH=________��
���� | K+ | Na+ | NH4+ | SO42- | NO3- | CI- |
Ũ��mol/L | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
(2)��֪����������NO�����ɷ�ӦΪ:N2(g)+ O2(g) ![]() 2NO(g) ��H>0���£������ܱ������У�����˵���У���˵���÷�Ӧ�ﵽ��ѧƽ��״̬����______________��
2NO(g) ��H>0���£������ܱ������У�����˵���У���˵���÷�Ӧ�ﵽ��ѧƽ��״̬����______________��
A.���������ܶȲ��ٱ仯 B.��������ѹǿ���ٱ仯
C.������ת���ʲ��ٱ仯 D.N2��O2��NO�����ʵ���֮��Ϊ1: 1: 2
(3)Ϊ����SO2 ���ŷţ�����ȡ�Ĵ�ʩ��:
�ٽ�úת��Ϊ�������ȼ�ϡ�
��֪:H2(g)+1/2O2(g)==H2O(g) ��H= -241.8kJ/mol
C(s)+1/2O2(g)==CO(g) ��H=-110.5kJ/mol
д����̿��ˮ������Ӧ���Ȼ�ѧ����ʽ:__________________________��
��ϴ�Ӻ�SO2�����������п���Ϊϴ�Ӻ�SO2������ϴ�Ӽ���________��
A.Ũ��ˮ B.̼�����Ʊ�����Һ
C.FeCl2������Һ D.����CaCl2������Һ
(4)����ʹ���Ҵ����Ͳ����ܼ���NOx���ŷţ���ʹNOx����Ч������Ϊ�����������Ҫ���⡣ij�о���С����ʵ������Ag-ZSM-5Ϊ���������NOת��ΪN2��ת�������¶ȱ仯�����ͼ��ʾ������ʹ��CO���¶ȳ���775K������NO�ķֽ��ʽ��ͣ�����ܵ�ԭ��Ϊ____________����n(NO)/n(CO)=1�������£�Ϊ���õij�ȥNOx���ʣ�Ӧ���Ƶ�����¶���______K���ҡ�

(5)�����ŷŵĵ������úȼ�ղ����Ķ��������ǵ������������ġ�������ס�������̿�ɴ���������Ⱦ��NO����5L�ܱ������м���NO �ͻ���̿(����������)��һ����������������E��F�����¶ȷֱ���T1���T2��ʱ����ø�����ƽ��ʱ���ʵ���(n/mol)���±�:

��д��NO�����̿��Ӧ�Ļ�ѧ����ʽ____________________________��
����T12����÷�Ӧ�ġ�H_____________0(�>������<����=��)��
��������ӦT1��ʱ�ﵽ��ѧƽ�����ͨ��0.lmol NO���壬��ﵽ�»�ѧƽ��ʱNO��ת����Ϊ___________________��