题目内容
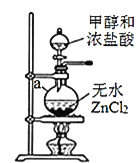
【题目】(1)12g碳与适量水蒸气反应生成CO和H2,需吸收131.3KJ热量,此反应的热化学方程式为______________________________。
(2)已知以下的热化学反应方程式:
①2CO(g)+O2(g)=2CO2(g) △H=-566kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H=-484kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890kJ/mol
则:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=______。
(3)已知H2(g)+Br2(l)=2HBr(g) △H=-102kJ/mol,其他的相关数据如下表:
H2(g) | Br2(l) | HBr(g) | |
1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
则表中a为_______。
【答案】C(s)+ H2O(l) =CO(g) + H2(g) ; ΔH=+131.3KJ·mol-1 +160 KJ·mol-1 200
【解析】
(1)根据题目所给信息写出配平方程式,并计算焓变,标明物质状态即可得到热化学方程式;
(2)根据盖斯定律,方程式叠加得到目标方程式,方程式如何叠加则焓变就如何叠加,得到目标反应的焓变;
(3)反应的焓变等于反应物键能之和减去生成物键能之和。
(1)碳与适量水蒸气反应生成![]() 和
和![]() ,即
,即![]() ,再根据12g(1mol)碳吸收131.3KJ热量,得到该反应的焓变为+131.3KJ/mol,
,再根据12g(1mol)碳吸收131.3KJ热量,得到该反应的焓变为+131.3KJ/mol,
故答案为:![]() ;
;
(2)③-①-②得到目标方程式,故目标反应的焓变等于![]() ,
,
故答案为:+160 KJ·mol-1;
(3)![]() ,解得a=200,
,解得a=200,
故答案为:200。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】现使用酸碱中和滴定法测定市售白醋的总酸量g/100ml![]() 。
。
(1)量取10.00ml食用白醋,在烧杯中用水稀释后转移到100mL容量瓶中定容,摇匀即得待测白醋溶液。
(2)用___(填仪器名称)取待测白醋溶液20.00ml于锥形瓶中,向其中滴加2滴酚酞。
(3)读取盛装0.1000mol/LNaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为___mL。滴定终点的现象:___,停止滴定,记录NaOH溶液的终读数,计算实验所用NaOH溶液总体积记录于下表,重复滴定4次。
![]()
(4)实验记录数据(ml)
滴定次数 | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH) | 15.95 | 15.00 | 15.05 | 14.95 |
(5)数据处理与讨论:
A.甲同学在处理数据时计算得:平均消耗的NaOH溶液的体积__ml,按正确数据处理,可得市售白醋总酸量![]() __g/100ml。
__g/100ml。
B.在本实验的滴定过程中,下列操作对实验结果的影响是(填写“偏大”、“偏小”或“无影响”)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗___;
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失___;
c.锥形瓶中加入待测白醋溶液后,再加少量水___。