题目内容
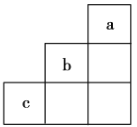
【题目】短周期元素a、b、c在周期表中的相对位置如图所示,下列有关这三种元素的叙述正确的是
A.b的氢化物很稳定
B.a是一种活泼的非金属元素
C.c的最高价氧化物对应的水化物是弱酸
D.b的单质不能与H2O反应
【答案】A
【解析】
由短周期中元素a、b、c在周期表中的位置可知,a为He元素,b为F元素,c为S元素。
A. 非金属性越强,对应氢化物越稳定;
B. He的化学性质稳定;
C. 硫酸属于强酸;
D. F2与水反应产生HF和O2。
由短周期中元素a、b、c在周期表中的位置可知,a为He元素,b为F元素,c为S元素。
A. F元素非金属性最强,对应氢化物很稳定,A正确;
B. He原子最外层为稳定结构,化学性质不活泼,B错误;
C. c的最高价氧化物的水化物是硫酸,硫酸是二元强酸,C错误;
D. F2与水剧烈反应产生HF和O2,反应方程式为2F2+2H2O=4HF+O2,D错误;
故合理选项是A。

练习册系列答案
相关题目