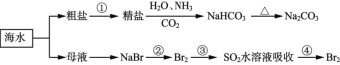
题目内容
【题目】现有①BaCl2、②金刚石、③醋酸钠、④Na2SO4、⑤干冰、⑥碘六种物质,按下列要求回答问题:
(1)熔化时不需要破坏化学键的是______(填序号,下同),熔化时需要破坏共价键的是______,熔点最高的是______,熔点最低的是______。
(2)属于离子晶体的是______(填序号,下同),只含有离子键的物质是______。
(3)①的电子式是______,⑤的电子式是______。
【答案】⑤⑥ ② ② ⑤ ①③④ ① ![]()
![]()
【解析】
(1)分子晶体熔化时不需要破坏化学键;原子晶体熔化时需要破坏共价键。
(2)固体物质中含有离子键的为离子晶体。
(3)①为离子化合物,只含有离子键;⑤为共价化合物。
(1)⑤干冰、⑥碘为分子晶体,分子晶体熔化时不需要破坏化学键;②金刚石为原子晶体,原子晶体熔化时需要破坏共价键,且金刚石的熔点比离子晶体①BaCl2、③醋酸钠、④Na2SO4高;熔点最低的为⑤干冰,常温下为气体。
(2)固体物质中含有离子键的为①BaCl2、③醋酸钠、④Na2SO4,属于离子晶体;①BaCl2只含有离子键。
(3)①为离子化合物,只含有离子键,电子式是![]() ;⑤为共价化合物,电子式为
;⑤为共价化合物,电子式为![]() 。
。

【题目】研究电解质在水溶液中的平衡能了解它的存在形式。
(1)已知部分弱酸的电离常数如下表:
化学式 | HF | H2CO3 | H2S |
电离平衡常数K(25℃) |
|
|
|
①写出H2S的Ka1的表达式:________________。
②常温下,pH相同的三种溶液NaF、Na2CO3、Na2S,物质的量浓度最小的是_______。
③将过量H2S通入Na2CO3溶液,反应的离子方程式是_______________。
(2)室温下,用0.100 mol·L-1 盐酸溶液滴定20.00 mL 0.100 mol·L-1 的氨水溶液,滴定曲线如图所示。(忽略溶液体积的变化,①②填“>”“<”或“=”)
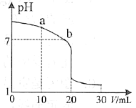
①a点所示的溶液中c(NH3·H2O)___________c(Cl-)。
②b点所示的溶液中c(Cl-)___________c(NH4+)。
③室温下pH=11的氨水与pH=5的NH4Cl溶液中,由水电离出的c(H+)之比为__________。
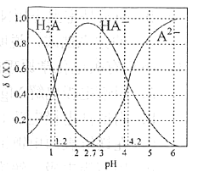
(3)二元弱酸H2A溶液中H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示。则H2A第二级电离平衡常数Ka2=___________。