题目内容
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
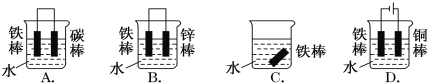
(1)下列哪个装置可防止铁棒被腐蚀________________。
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:
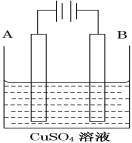
①铁件应与电源的________极相连(写正或负),B电极的电极反应式是______。
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为10.24 g,则电镀时电路中通过的电子为________mol。
③电镀结束后CuSO4溶液的浓度______(填变大,变小,不变)
④镀层破损后,铁不易被腐蚀的是___________(填序号)。
A 镀铜铁 B 镀锌铁 C 镀锡铁
【答案】BD 负 Cu2++2e_= Cu 0.16 不变 B
【解析】
在铁件上镀铜时,铜作阳极,与正极相连,铁件作阴极,Cu2+得电子生成Cu:Cu2++2e-=Cu,镀层破损后,镀铜铁形成的原电池中铁作负极,腐蚀加快,镀锌铁形成的原电池中铁作正极被保护。
(1)铁作原电池的正极或电解池的阴极时可防止被腐蚀,B为原电池,锌作负极被腐蚀,铁作正极被保护,D为电解池,铁与电源的负极相连,作阴极被保护;
故答案为 BD
(2)①在铁件上镀铜时,铜作阳极,与正极相连,铁棒作阴极,B电极为阴极,阴极发生还原反应,Cu2+得电子生成Cu:Cu2++2e-=Cu;
②A极为阳极,发生氧化反应阳极反应离子方程式:Cu-2e-=Cu2+,故阳极固体质量减少,阴极固体质量增加,二者质量差为10.24 g,则阴极表面增加的铜的质量为5.12g,转换为物质的量为0.08mol,已知每生成1mol铜转移2mol电子,故电路中通过的电子为0.16mol;
③A极为阳极,发生氧化反应阳极反应离子方程式:Cu-2e-=Cu2+,这样溶液中Cu离子的浓度就不会改变;
④镀层破损后,镀铜铁、镀锡铁形成的原电池中铁作负极,腐蚀加快,镀锌铁形成的原电池中铁作正极被保护;
故答案为负 Cu2++2e-= Cu 0.16 不变 B。

【题目】化学反应中不仅有物质变化而且伴随着能量变化。
(1)以下实验中属于吸热反应的是________(填序号)。
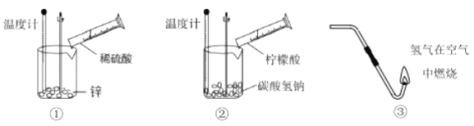
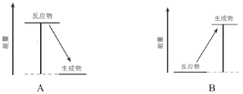
(2)下图中,表示放热反应能量变化的是_______(填字母)。
(3)从微观角度分析化学反应中能量变化的原因:

图中①和②分别为_______、_______(填“吸收”或“释放”)。氢气与氧气反应生成1mol水蒸气时,释放________kJ能量。
(4)当前,很多地区倡导用天然气替代煤作为家用燃料,根据下表从尽可能多的角度分析其原因是__。
燃料 | 燃烧释放的能量(每1千克) |
天然气 | 55812kJ |
煤 | 20908kJ |
【题目】根据下表提供的数据,下列判断正确的是![]()
化学式 | 电离常数 |
HF |
|
|
|
| |
HClO |
|
A.同温同浓度下,溶液的pH值:![]()
B.结合![]() 的能力:
的能力:![]()
C.碳酸钠溶液中加入少量氢氟酸的离子方程式:![]()
D.次氯酸钠溶液中通入少量二氧化碳的离子方程式:![]()