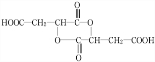
题目内容
10.FeCl3在现代工业生产中应用广泛.某化学研究性学习小组模拟工业生产流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S.Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
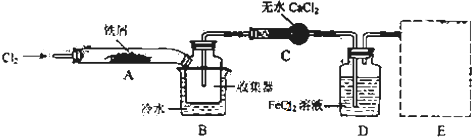
①检查装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成
④…
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封
请回答下列问题:
(1)装置A中反应的化学方程式为2Fe+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A的右端.要使沉积得FeCl3进入收集器,第④步操作是在沉积的FeCl3固体下方加热
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)②⑤
(4)装置B中的冷水作用为冷却,使FeCl3沉积,便于收集产品;装置C的名称为干燥管;装置D中FeCl2全部反应完后,因为失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂:KMnO4溶液;在虚线框内画出尾气吸收装置E并注明试剂
Ⅱ.该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液.
(5)FeCl3与H2S反应的离子方程式为2Fe3++H2S=2Fe2++S↓+2H+
(6)电解池中H+在阴极放电产生H2,阳极的电极反应为Fe2+-e-=Fe3+.
分析 Ⅰ.装置A中铁与氯气反应,反应为:2Fe+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3,B中的冷水作用为是冷却FeCl3使其沉积,便于收集产品;为防止外界空气中的水蒸气进入装置使FeCl3潮解,所以用装置C无水氯化钙来吸水,装置D中用FeCl2吸收Cl2时的反应离子方程式2Fe2++Cl2═2Fe3++2Cl-,用装置D中的副产品FeCl3溶液吸收H2S,离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,用氢氧化钠溶液吸收的是氯气,不用考虑防倒吸,所以装置E为氢氧化钠溶液吸收氯气.
(1)装置A中铁与氯气反应生成氯化铁;
(2)要使沉积的FeCl3进入收集器,根据FeCl3加热易升华的性质;
(3)防止FeCl3潮解,不与水蒸气接触;
(4)B中的冷水作用为是冷却FeCl3使其沉积,便于收集产品;装置C的名称为干燥管;检验FeCl2是否失效应检验FeCl2是否存在,可以用KMnO4溶液检验;用氢氧化钠溶液吸收的是氯气,不用考虑防倒吸;
Ⅱ.(5)三价铁具有氧化性,硫化氢具有还原性,二者之间发生氧化还原反应;
(6)电解氯化亚铁时,阴极阳离子得到电子发生还原反应;阳极阳离子失去电子发生氧化反应.
解答 解:Ⅰ.(1)氯气具有强氧化性,将变价铁氧化成高价铁,生成氯化铁,所以装置A中铁与氯气反应生成氯化铁,反应为2Fe+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3,
故答案为:2Fe+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3;
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,第④步操作是对FeCl3加热发生升华使沉积的FeCl3进入收集器,
故答案为:在沉积的FeCl3固体下方加热;
(3)为防止FeCl3潮解所采取的措施有②通入干燥的Cl2⑤用干燥的N2赶尽Cl2,故选:②⑤;
(4)B中的冷水作用为是冷却FeCl3使其沉积,便于收集产品,装置C的名称为干燥管;
检验FeCl2是否失效,应检验FeCl2是否存在,可以用KMnO4溶液检验;
用氢氧化钠溶液吸收的是氯气,不用考虑防倒吸,
故答案为:冷却,使FeCl3沉积,便于收集产品;干燥管;KMnO4溶液;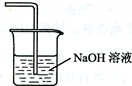 ;
;
Ⅱ.(5)三价铁具有氧化性,硫化氢具有还原性,二者之间发生氧化还原反应:2FeCl3+3H2S=2FeCl2+6HCl+3S↓,离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,
故答案为:2Fe3++H2S=2Fe2++S↓+2H+;
(6)电解氯化亚铁时,阴极发生氢离子得电子的还原反应,2H++2e-═H 2↑,阳极亚铁离子发生失电子的氧化反应:Fe2+-e-=Fe3+,
故答案为:Fe2+-e-=Fe3+.
点评 本题考查了制备无水FeCl3实验操作和实验设计,题目难度中等,侧重考查铁、氯、硫及其化合物的性质应用、实验基本操作的分析判断、实验现象的推断和应用,试题综合性较强,有利于培养学生灵活应用基础知识的能力.

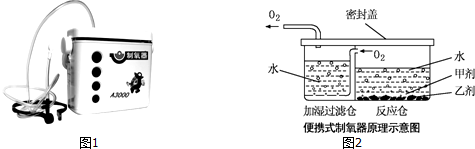
【提出问题】甲剂的化学成分是什么?
【阅资料】过碳酸钠是白色颗粒状固体,溶于水时,生成碳酸钠和过氧化氢,可用于制取氧气.
【设计与实验】小雨把甲剂和乙剂带到实验室与黄老师共同探究.在老师的指导下,验证出甲剂是一种钠盐后,小雨接着进行如下实验:
[实验一]用甲剂和乙剂制取并验证氧气.
(1)根据图2得出:组装气体发生装置时应选择图3所示的仪器:ABCFG 或ACEG(填字母),该装置还可用于制取的气体是氢气、二氧化碳;
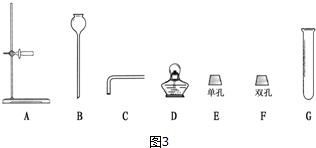
(2)装置连接完毕,装药品前应先检查装置的气密性;
(3)小雨认为氧气是由过氧化氢在乙剂催化下产生的,其化学方程式为2H2O2 $\frac{\underline{\;乙剂\;}}{\;}$2H2O+O2↑;
(4)检验氧气的方法是将带火星的木条伸入集气瓶内,木条复燃.
[实验二]检验上述反应后的溶液中是否含有碳酸根离子.
| 检验步骤 | 实验操作 | 实验现象 | 结论 | |
| 步骤一 | 取少量反应后的溶液,加入稀盐酸 | 有气泡产生 | ||
| 步骤二 | 将步骤一产生的气体通入澄清石灰水 | 澄清石灰水变浑浊 |
【反思与评价】小方认为小雨的结论不够严密,你认为严密的结论应该是甲剂一定含有钠、碳和氧三种元素(或甲剂可能是过碳酸钠).
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -1l6 |
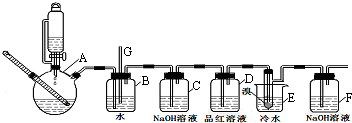
(1)实验开始之前必要的操作是检查装置的气密性.
(2)仪器A的名称为三颈瓶.
(3)实验过程中,若发现装置B中水沿导管G上升,则需进行的操作是停止加热,向烧杯E中加适量温水.
(4)装置D中品红溶液的作用是验证二氧化硫是否被除尽.
(5)反应过程中应用冷水冷却装置E,其主要目的是减少液溴挥发.
(6)判断该制备反应已经结束的最简单方法是装置E中小试管内的液体由红棕色变为无色;结果学生发现反应结束时,无水乙醇消耗量大大超过理论值,其原因是有副反应发生或反应过于剧烈,一部分乙烯没有充分反应就逸出(答出其中两条即可).

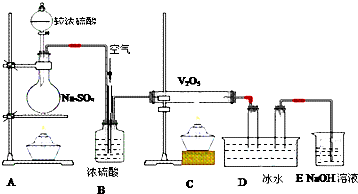
已知:SiCl4熔点为-70.0℃,沸点为57.7℃,且遇水易水解.
(1)装置C中的试剂是浓硫酸:装置F的作用为防止F右端的水蒸气进入E与四氯化硅反应,造成产物不纯.
(2)装置A中发生反应的离子方程式为:MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑.A装置中,有一处明显错误是无石棉网.
(3)装置D的硬质玻璃管中发生反应的化学方程式是SiO2+2C+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SiCl4+2CO.
(4)G中吸收气体一段时间后,吸收液中肯定存在OH-、Cl-和SO42-.为探究该吸收液中可能存在的其它酸根离子(忽略空气中CO2的影响).
【提出假设】假设1:只有SO32-;假设2:既无SO32-也无ClO-:假设3:只有ClO-.
【设计方案,进行实验】可供选择的实验试剂有:3mol/L H2SO4溶液、1mol/L NaOH溶液、溴水、品红溶液、0.01mol/L KMnO4溶液、淀粉-KI溶液.
各取少量吸收液于a、b、c三支试管中,分别滴加适量的3mol/LH2SO4溶液后,进行下列实验.请完成下表:
| 序号 | 操作 | 可能出现的现象 | 结论 |
| ① | 向a试管中滴加几滴0.01mol/L的KMnO4(或溴水)溶液 | 若溶液褪色 | 则假设1成立 |
| 若溶液不褪色 | 则假设2或3成立 | ||
| ② | 向b试管中滴加几滴品红溶液 | 若溶液褪色 | 则假设1或3成立 |
| 若溶液不褪色 | 假设2成立 | ||
| ③ | 向C试管中滴加几滴淀粉-KI溶液 | 若溶液变为蓝色 | 假设3成立 |
| A. | 已知可逆反应:2SO2+O2?2SO3,当O2的消耗速率与SO3的消耗速率之比为1:2时,表明该可逆反应达到化学平衡状态 | |
| B. | 由Zn、Cu、稀硫酸组成的原电池,负极为Zn,发生还原反应,电极反应式为:Zn-2e-=Zn2+ | |
| C. | 工业上金属Mg、Al都是用电解熔融的氯化物制得的 | |
| D. | 甲苯的一氯代物有4种,则甲苯与足量H2发生加成反应后所得到的有机产物的一氯代物也只有4种 |
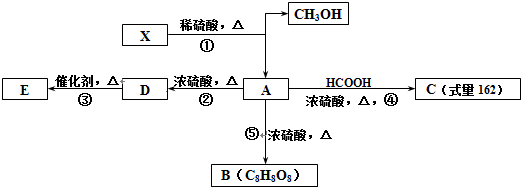
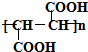
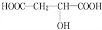 +HCOOH$?_{△}^{浓硫酸}$
+HCOOH$?_{△}^{浓硫酸}$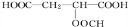 +H2O
+H2O