题目内容
18.下列实验装置或操作正确的是( )| A. | 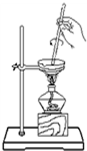 从碘水中分离出碘 | B. | 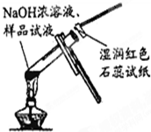 检验试液中NH4+的存在 | ||
| C. |  干燥SO2气体 | D. | 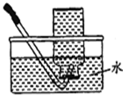 收集HCl气体 |
分析 A.碘易升华,不能利用蒸发;
B.铵盐与NaOH反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝;
C.二氧化硫与碱石灰反应;
D.HCl极易溶于水.
解答 解:A.碘易升华,不能利用蒸发,应选择萃取、蒸馏分离出碘,故A错误;
B.铵盐与NaOH反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝,图中试纸变蓝,可检验试液中NH4+的存在,故B正确;
C.二氧化硫与碱石灰反应,则干燥试剂不合理,应利用浓硫酸及洗气瓶干燥二氧化硫,故C错误;
D.HCl极易溶于水,不能利用排水法收集,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、离子检验、气体的干燥及收集等,把握物质的性质及实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
8.现有常温下水电离出的c(H+)均为1×10-11mol/L的4种溶液:①HCl溶液;②CH3COOH溶液;③NaOH溶液;④氨水.有关上述溶液的比较中,正确的是( )
| A. | 向等体积溶液中分别加水稀释100倍后,溶液的pH:③>④>②>① | |
| B. | 等体积的①、②、③溶液分别与足量铝粉反应,生成H2的量①最小 | |
| C. | ②、③溶液等体积混合后,溶液显碱性 | |
| D. | ①、④溶液混合若pH=7,则消耗溶液的体积:④>① |
9.下列说法正确的是( )


| A. | 用右图所示方法可保护钢闸门不被腐蚀 | |
| B. | SiO2(s)+2C(s)═Si(s)+2CO(g)在常温下不能自发进行,则该反应的△H>0 | |
| C. | 常温下,NH4Cl溶液加水稀释,$\frac{{c(N{H_3}•{H_2}O)•c({H^+})}}{{c(N{H_4}^+)}}$增大 | |
| D. | C(s)+H2O(g)?CO(g)+H2(g)(△H>0),其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动 |
13.下列物质或指定物质主要成分与化学式对应正确的是( )
| A. | 明矾--Al2(SO4)3•12H2O | B. | 漂白粉--NaClO | ||
| C. | 纯碱--NaHCO3 | D. | 水煤气--CO、H2 |
3.短周期主族元素W、R、X、Y、Z的原子序数依次增大,W的原子半径是周期表中所有元素中最小的,R是地壳中含量最多的元素,X与W同主族,Y是最外层电子数是最内层电子数的3倍.下列说法正确的是( )
| A. | 原子半径:R<Y<Z | B. | 简单氢化物的热稳定性:R>Y | ||
| C. | R与Y只能形成一种化合物 | D. | 最高价氧化物的水化物酸性:Y>Z |
10.下列说法正确的是( )
| A. | 因为反应物浓度越大,反应速率越快,所以常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 | |
| B. | 增大反应物浓度可加快反应速度,因此用浓硫酸与铁反应能增大生成H2的速率 | |
| C. | 对化学反应速率起决定性作用的因素是参加反应的各物质的性质 | |
| D. | 化学反应速率也可以用单位时间内固体物质的消耗量或者气体物质的生成量来表示 |
7.某W固体可能有①CuCl2②AlCl3③NaNO2④NH4Cl⑤AgNO3⑥FeCl2⑦NaOH中的一种或几种组成,现有某学习兴趣小组对此W固体进行实验探究分析,得到如下的实验流程,则对原W固体组成的分析不正确的是( )
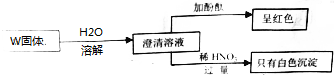

| A. | 一定不存在③⑥ | B. | 可能存在①② | C. | 一定存在①④⑦ | D. | 至少存在④⑤⑦ |
 50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中方程的热量可计算中和热,回答下列问题:
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中方程的热量可计算中和热,回答下列问题: 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )