题目内容
16.已知下列热化学方程式:①H2O(l)═H2(g)+$\frac{1}{2}$O2(g)△H=+285.8kJ/mol
②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/mol
③C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5kJ/mol
④C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
回答下列问题:
(1)上述反应中属于吸热反应的是①.
(2)C的燃烧热为393.5kJ/mol.(取正值)
(3)燃烧10g H2生成液态水,放出的热量为1429kJ.
(4)写出CO燃烧的热化学方程式CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283kJ/mol,
(5)写出制水煤气的热化学方程式C(s)+H2O(g)=CO(g)+H2(g)△H=-396.3kJ/mol.
分析 (1)焓变△H<0为放热反应,△H>0为吸热反应;
(2)燃烧热是指1mol可燃物完全燃烧生成稳定氧化物放出的热量,单位为kJ/mol;
(3)由H2O(l)═H2(g)+$\frac{1}{2}$O2(g)△H=+285.8kJ/mol,可知1mol氢气燃烧生成液态水放出的热量为285.8kJ,根据n=$\frac{m}{M}$计算氢气的物质的量,进而计算放出的热量;
(4)已知:③C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5kJ/mol
④C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
由盖斯定律,④-③可得CO燃烧的热化学方程式;
(5)制水煤气发生反应:C(s)+H2O(g)=CO(g)+H2(g),根据盖斯定律③-①可得C(s)+H2O(g)=CO(g)+H2(g),反应热也进行相应计算,可得热化学方程式.
解答 解:(1)焓变△H<0为放热反应,△H>0为吸热反应,故上述反应中①属于吸热反应,故答案为:①;
(2)燃烧热是指1mol可燃物完全燃烧生成稳定氧化物放出的热量,单位为kJ/mol,由④C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol,可知碳的燃烧热为:393.5kJ/mol,故答案为:393.5kJ/mol;
(3)由H2O(l)═H2(g)+$\frac{1}{2}$O2(g)△H=+285.8kJ/mol,可知1mol氢气燃烧生成液态水放出的热量为285.8kJ,10g氢气的物质的量为$\frac{10g}{2g/mol}$=5mol,燃烧生成液态水,放出的热量为 285.8kJ×$\frac{5mol}{1mol}$=1429kJ,故答案为:1429kJ;
(4)已知:③C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5kJ/mol
④C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
由盖斯定律,④-③可得CO燃烧的热化学方程式:CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283kJ/mol,
故答案为:CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283kJ/mol;
(5)制水煤气发生反应:C(s)+H2O(g)=CO(g)+H2(g),根据盖斯定律③-①可得C(s)+H2O(g)=CO(g)+H2(g),则△H=(-110.5kJ/mol)-285.8kJ/mol=-396.3kJ/mol,故热化学方程式为:C(s)+H2O(g)=CO(g)+H2(g),则△H=-396.3kJ/mol,
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=-396.3kJ/mol.
点评 本题考查热化学方程式书写、反应热计算、燃烧热等,比较基础,注意运用盖斯定律书写热化学方程式、进行反应热计算.

Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
(1)基态Ti3+的未成对电子数有1个.
(2)LiBH4由Li+和BH4-构成,LiBH4中不存在的作用力有C(填标号).
A.离子键 B.共价键 C.金属键 D.配位键
(3)Li、B、H元素的电负性由大到小排列顺序为H>B>Li.
(4)分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料.X一定不是BC(填标号).
A.H2O B.CH4 C.HF D.CO(NH2)2
(5)钾、镁、氟形成的某化合物的晶体结构为K+在立方晶胞的中心,Mg2+在晶胞的8个顶角,F-处于晶胞的棱边中心.由钾、镁、氟形成的该化合物的化学式为KMgF3,每个K+与12个F-配位.
(6)判断含氧酸酸性强弱的一条经验规律是含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.如下表所示:含氧酸酸性强弱与非羟基氧原子数的关系
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 | Cl-OH | 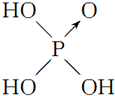 |  | 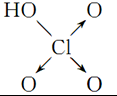 |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
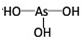 .H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
.H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:①H3PO3+2NaOH=Na2HPO3+2H2O,
②H3AsO3+3NaOH=Na3AsO3+3H2O.
| A. | 将铜丝插入浓硫酸加热,反应后把水加入反应器中,观察硫酸铜溶液的颜色 | |
| B. | 常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成 | |
| C. | 金属钠放入硫酸铜溶液中可以置换出金属铜 | |
| D. | 将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿 |
| 选项 | 离子组 | 所加试剂 | 离子方程式 |
| A | Mg2+、Fe3+、NO3- | KSCN溶液 | Fe3++3SCN-═Fe(SCN)3↓ |
| B | NH4+、HCO3-、Cl- | 过量NaOH溶液 | HCO3-+OH-═CO32-+H2O |
| C | Fe2+、Cl-、H+ | KNO3溶液 | 3Fe2++NO3-+4H+═NO↑+2H2O+3Fe3+ |
| D | K+、H+、C6H5O- | Na2CO3溶液 | 2H++CO32-═CO2↑+H2O |
| A. | A | B. | B | C. | C | D. | D |

| A. | 烧杯中溶液逐渐呈蓝色 | B. | 锌片逐渐溶解 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 该装置能够将电能转化为化学能 |
| A. | 常温下,醋酸钠与醋酸的混合溶液pH=7,c(Na+)=c(CH3COO-) | |
| B. | 0.1 mol/L Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | |
| C. | 常温下,将pH=1的醋酸溶液稀释100倍后,水电离的c(H+)=10-11mol/L | |
| D. | 0.1mol/L NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) |
| A. | 聚氯乙烯分子中含碳碳双键 | B. | 以淀粉为原料可制取乙酸乙酯 | ||
| C. | 戊烷有3种同分异构体 | D. | 油脂的皂化反应属于水解反应 |