题目内容
【题目】请按要求回答下列问题:
(1)纯水在100℃时pH=6,该温度下1mol·L-1的NaOH溶液中,由水电离出的c(OH-)=__mol·L-1。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为__,由水电离出的c(OH-)=___mol·L-1。
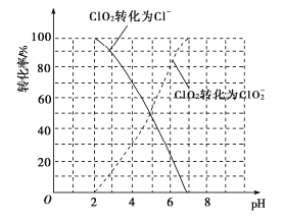
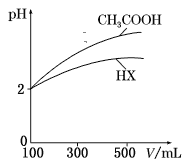
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离常数___(填“大于”“小于”或“等于”)CH3COOH的电离常数。理由是___。
(4)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式 | 电离常数(25℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,有等pH的a.NaCN溶液、b.Na2CO3溶液和c.CH3COONa溶液,三溶液的浓度由大到小的顺序为___。(用a、b、c表示)
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为___。
③25℃时,等浓度的HCN和NaCN混合溶液显___性。(酸、碱、中)
(5)室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
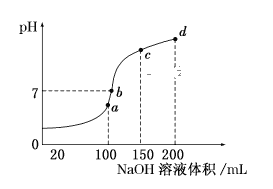
试分析图中a、b、c、d四个点,水的电离程度最大的是__;在b点,溶液中各离子浓度由大到小的排列顺序是__。
【答案】10-12 CO32-+H2O![]() OH-+HCO3- 10-3 小于 稀释相同的倍数,一元酸HX的pH变化比CH3COOH小 cab NaCN+CO2+H2O=NaHCO3 +HCN 碱 a (Na+)>(SO42-)>(NH4+)>(OH-)=(H+)
OH-+HCO3- 10-3 小于 稀释相同的倍数,一元酸HX的pH变化比CH3COOH小 cab NaCN+CO2+H2O=NaHCO3 +HCN 碱 a (Na+)>(SO42-)>(NH4+)>(OH-)=(H+)
【解析】
(1)纯水在T℃时,pH=6,说明此时水的离子积常数为10-12,该温度下1molL-1的NaOH溶液中,氢离子由水电离产生;
(2)由水电离出的c(OH-)等于溶液中氢氧根离子的浓度;
(3)根据图象可知,稀释相同倍数时,一元酸HX的pH变化量比CH3COOH的小,这说明HX存在电离平衡,因此HX为弱酸,并且酸性比CH3COOH还弱;
(4)①电离常数越大酸性越强,酸性越弱相应的钠盐越容易水解,等pH的NaCN溶液、Na2CO3溶液和CH3COONa溶液中,越容易水解,浓度越小;
②强碱弱酸盐对应的酸的酸性越弱,其水解程度就越大,pH越大,弱酸的电离平衡常数越小;
③NaCN水解显碱性;HCN电离显酸性,两者混合,因HCN的电离能力比CN-离子的水解能力弱,所以溶液显碱性;
(5)酸或碱抑制水电离,含有弱离子的盐促进水电离,以此解答。
(1)纯水在T℃时,pH=6,即c(H+)=c(OH-)=10-6,可知Kw=10-12,1mol·L-1的NaOH溶液中c(OH-)=1mol/L,由水电离出的c(OH-)取决于溶液中的c(H+),即c(OH-)水=c(H+)= ![]() =10-12mol·L-1;
=10-12mol·L-1;
(2)25 ℃时,向水中加入少量碳酸钠固体,碳酸根水解,得到pH为11的溶液,c(H+)=10-11mol/L,则其水解的离子方程式为CO32-+H2O![]() HCO3-+OH-,其中由水电离出的c(OH-)等于溶液中氢氧根离子的浓度,即由水电离出的c(OH-)=
HCO3-+OH-,其中由水电离出的c(OH-)等于溶液中氢氧根离子的浓度,即由水电离出的c(OH-)=![]() =
= ![]() mol/L=10-3mol·L-1;
mol/L=10-3mol·L-1;
(3)根据图象可知,稀释相同倍数时,一元酸HX的pH变化量比CH3COOH的小,这说明HX存在电离平衡,因此HX为弱酸,并且酸性比CH3COOH还弱,故HX的电离常数小于CH3COOH的电离常数,理由是:稀释相同的倍数,一元酸HX的pH变化比CH3COOH小;
(4)①电离常数越大酸性越强,酸性越弱相应的钠盐越容易水解。根据表中数据可知酸性强弱顺序为CH3COOH>H2CO3>HCN>HCO3-,所以25 ℃时,等pH的NaCN溶液、Na2CO3溶液和CH3COONa溶液中,越容易水解,浓度越小,三溶液的浓度由大到小的顺序为CH3COONa>NaCN>Na2CO3,正确答案是:cab;
②强碱弱酸盐对应的酸的酸性越弱,其水解程度就越大,pH越大,弱酸的电离平衡常数越小。其中Na2CO3对应的是K2=5.6×10-11,H2CO3的K1大于K(HCN),K2小于K(HCN),因此向NaCN溶液中通入少量的CO2,产物应是NaHCO3,方程式为:NaCN+CO2+H2O=NaHCO3 +HCN;
③NaCN水解显碱性;HCN电离显酸性,两者混合,因HCN的电离能力比CN-离子的水解能力弱,所以溶液显碱性;
(5)酸或碱抑制水电离,含有弱离子的盐促进水电离,a点溶质为 (NH4)2SO4、Na2SO4;/span>b点溶质为(NH4)2SO4、Na2SO4、NH3H2O,但一水合氨浓度小于c点;c点溶质为(NH4)2SO4、Na2SO4、NH3H2O,但一水合氨浓度小于d点,d点溶质为Na2SO4、NH3 H2O,溶液中酸浓度或碱浓度越大,抑制水电离程度越大,所以a点促进水电离、bcd点抑制水电离,且抑制水电离程度b<c<d,则水的电离程度最大点是a点;b点溶液为中性,溶质为(NH4)2SO4与Na2SO4、NH3H2O,V(NaOH)>V(NH4HSO4),铵根离子水解,则离子浓度大小为c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)。

 习题精选系列答案
习题精选系列答案【题目】某学生用0.10 mol·L-1标准NaOH溶液滴定某浓度的盐酸。记录数据如下:
实验序号 | 待测液体积(mL) | 所消耗NaOH标准液的体积(mL) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.50 | 20.54 |
2 | 20.00 | 6.00 | 26.00 |
3 | 20.00 | 1.40 | 21.36 |
(1)盐酸的物质的量浓度为_____。
(2)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是_____(填“偏高”或“偏低”或“无影响”)。
(3)下列有关实验的说法正确的是______。
A.在测定中和反应的反应热实验中,至少要读两次温度
B.可用pH试纸测定新制氯水中的pH
C.中和滴定实验中,洗净后的锥形瓶不需要干燥
D.向CH3COONa溶液中滴入石蕊试液,溶液变蓝
E.向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS)
(4)常温下,pH=5的盐酸和pH=9的氢氧化钠溶液以体积比9∶11混合,则混合液的pH=_________。