题目内容
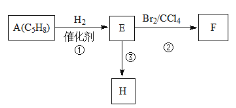
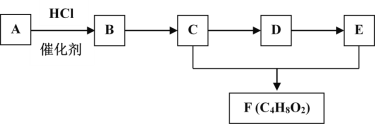
【题目】有机物A~F的转化关系如下图所示。已知A在标准状况下的密度为1.25gL—1,D能发生银镜反应,F是难溶于水且有芳香气味的油状液体。
请回答:
(1)A中官能团名称为________。
(2)C→D的反应类型是_________。
(3)A和E一定条件下也可生成F的化学方程式是_______。
(4)下列说法正确的是______。
A.A和B都能使酸性KMnO4褪色
B.D和E能用新制氢氧化铜悬浊液检验
C.可以用饱和碳酸钠溶液除去C、E和F混合物中的C、E
D.推测有机物F可能易溶于乙醇
【答案】碳碳双键 氧化反应 CH2=CH2+CH3COOH→CH3COOCH2CH3 B、C、D
【解析】
D能发生银镜反应,F是难溶于水且有芳香气味的油状液体,可知C为醇,E为羧酸,结合F的分子式为C4H8O2可知C为CH3CH2OH、D为CH3CHO、E为CH3COOH、F为CH3COOCH2CH3;A在标准状况下的密度为1.25gL—1,则A的摩尔质量为1.25gL—1×22.4L/mol=28g/mol,可知A为CH2=CH2,B为CH3CH2Cl,B→C发生的是卤代烃的碱性水解,据此分析解题。
D能发生银镜反应,F是难溶于水且有芳香气味的油状液体,可知C为醇,E为羧酸,结合F的分子式为C4H8O2可知C为CH3CH2OH、D为CH3CHO、E为CH3COOH、F为CH3COOCH2CH3;A在标准状况下的密度为1.25gL—1,则A的摩尔质量为1.25gL—1×22.4L/mol=28g/mol,可知A为CH2=CH2,B为CH3CH2Cl,B→C发生的是卤代烃的碱性水解;
(1)A为CH2=CH2,含有的官能团名称为碳碳双键;
(2)CH3CH2OH→CH3CHO发生的是醇的催化氧化,反应类型是氧化反应;
(3)CH2=CH2和CH3COOH一定条件下发生加成反应可生成CH3COOCH2CH3,反应的化学方程式是CH2=CH2+CH3COOH→CH3COOCH2CH3;
(4)A.A为乙烯,分子结构中含有碳碳双键,能使酸性KMnO4褪色,而B为氯乙烷,不含碳碳双键,不能使酸性KMnO4褪色,故A错误;
B.D为乙醛,和新制氢氧化铜悬浊液混合加热生成砖红色沉淀,而E为乙酸,能溶解新制氢氧化铜悬浊液,得到澄清的溶液,能鉴别,故B正确;
C.乙酸乙酯中混有乙酸和乙醇,可以加入饱和碳酸钠溶液,振荡、静置后分液,上层为乙酸乙酯,故C正确;
D.乙醇是良好的有机溶剂,乙酸乙酯易溶于乙醇,故D正确;
故答案为B、C、D。

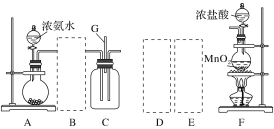
【题目】某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F为氨气和氯气的发生装置,C为纯净、干燥的氯气与氨气反应的装置。
备选装置 | ||
|
|
|
Ⅰ | Ⅱ | Ⅲ |
请回答下列问题:
(1)装置F中发生反应的离子方程式是___________________________________。
(2)装置A中的烧瓶内固体可选用________(填字母)。
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
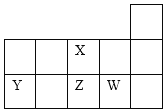
(3)虚线框内应添加必要的除杂装置,请从如图的备选装置中选择,并将编号填入下列空格:
B:________、D:________、E:________。
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:____________________________________;
(5)装置C内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案确定该白色固体中的阳离子:_______________________________________
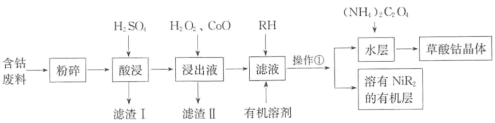
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某旧铍铜元件(含25%BeO、71%CuS、少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如图:

已知:Ⅰ.铍、铝元素的化学性质相似,单质铍与氢氧化钠溶液反应生成可溶于水的Na2BeO2
Ⅱ.常温下部分难溶物的溶度积常数如下表:
难溶物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
溶度积常数(Ksp) | 2.2×10-20 | 4.0×10-38 | 2.1×10-13 |
(1)滤液A的主要成分除NaOH外,还有___(填化学式),写出反应I中含铍化合物与过量盐酸反应的离子方程式:___。
(2)滤液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,最合理的实验步骤顺序为___(填字母)。
a.加入过量的氨水
b.通入过量的CO2
c.加入过量的NaOH
d.加入适量的HCl
e.洗涤
f.过滤
(3)①MnO2能将金属硫化物中的硫元素氧化为硫单质。写出反应Ⅱ中CuS发生反应的化学方程式:___。
②若用浓HNO3溶解金属硫化物,缺点是___(任写一条)。
(4)滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.01mol·L-1,逐滴加入稀氨水调节pH可将其依次分离,首先沉淀的是___(填离子符号),为使铜离子开始沉淀,常温下应调节溶液的pH大于___。
(5)电解NaCl-BeCl2混合熔盐可制备金属铍,如图是电解装置图。
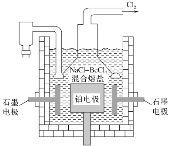
①石墨电极上的电极反应式为___。
②电解得到的Be蒸气中约含1%的Na蒸气,除去Be中少量Na的方法为___。
已知部分物质的熔、沸点如下表:
物质 | 熔点(K) | 沸点(K) |
Be | 1551 | 3243 |
Na | 370 | 1156 |
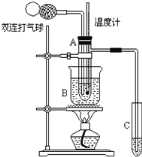
【题目】乙醛在催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体),已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下:
物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)_____________________________________________;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置:
①在实验开始时温度计水银球的位置应在_____________________;
②当试管A内的主要反应完成后温度计水银球的位置应在_______________,目的是________________________________________________;
(3)烧杯B内盛装的液体可以是________(写出一种即可);在实验的不同阶段,烧杯B的作用分别是_________________、______________________;
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案。所提供的药品有:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末。实验仪器任选。该方案为________________________________________。