题目内容
【题目】晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞。NaCl晶体的晶胞如右图所示。 随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定精确度也越来越高。现有一简单可行的测定方法,具体步骤如下:①将固体食盐研细,干燥后,准确称取m gNaCl固体并转移到定容仪器A中。②用滴定管向仪器A中加苯,并不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为VmL。回答下列问题:
⑴步骤①中A仪器最好用__________________(填仪器名称)。
⑵能否用胶头滴管代替步骤②中的滴定管______,其原因是____________。
⑶能否用水代替苯_______,其原因是______________________。
⑷经X射线衍射测得NaCl晶胞中最邻近的Na+ 和Cl- 平均距离为acm,则利用上述
方法测得的阿伏加德罗常数的表达式为NA=_______________________。

【答案】容量瓶 否 实验中需要准确量取苯的体积 否 若用水代替苯,NaCl会溶解,造成NaCl的体积不能准确测定出来 ![]()
【解析】
(1)容量瓶为定容仪器,能够较准确的测定体积;
(2)实验中需要准确量取苯的体积,因此不能用胶头滴管代替滴定管;
(3)NaCl会溶解,造成NaCl的体积不能准确测定出来;
(4)由实验中NaCl的质量与体积,可以得到NaCl晶体的密度,均摊法计算晶胞中Na+、Cl-数目,用阿伏伽德罗常数表示出晶胞质量,最近的Na+与Cl-间的平均距离为acm,则晶胞棱长=2a cm,而晶胞质量等于晶体密度与晶胞体积乘积,联立计算。
(1)能够较准确的测定NaCl固体体积,所以步骤①中仪器最好用容量瓶;
(2)实验中需要准确量取苯的体积,因此不能用胶头滴管代替滴定管;
(3)不能用水代替苯,若用水代替苯,NaCl会溶解,造成NaCl的体积不能准确测定出来;
(4)NaCl的密度为g/cm3,最近的Na+与Cl-间的平均距离为acm,则晶胞棱长=2a cm,NaCl晶胞的体积=(2a)3cm3,晶胞中Na+离子数目=1+12×![]() =4、Cl-数目=8×
=4、Cl-数目=8×![]() +6×
+6×![]() =4,则NaCl晶胞的质量=
=4,则NaCl晶胞的质量=![]() g=
g=![]() g/cm3×(2a)3cm3,整理得NA=
g/cm3×(2a)3cm3,整理得NA=![]() 。
。

【题目】利用铜萃取剂M,通过如下反应实现铜离子的富集:

(1)X难溶于水、易溶于有机溶剂,其晶体类型为________。
(2)M所含元素的电负性由大到小顺序为_______,N原子以_____轨道与O原子形成σ键。
(3)上述反应中断裂和生成的化学键有______(填序号)。
a.离子键
b.配位键
c.金属键
d.范德华力
e.共价键
(4)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是_____。
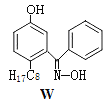
(5)基态Cu2+的外围电子排布式为________,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。判断Sc3+、Zn2+的水合离子为无色的依据是___________。
离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |