题目内容
6.混合物是由氯化钠、氯化镁、氯化铝组成,已知钠、镁、铝三种元素的质量比为23:16:9,计算:(1)氯化钠、氯化镁、氯化铝三种物质的物质的量之比为多少?
(2)当氯离子为1mol时,混合物的质量是多少?
分析 (1)设Na、Mg、Al三种元素的质量分别23g、16g、9g,根据n=$\frac{m}{M}$计算各自物质的量,根据原子守恒计算NaCl、MgCl2、AlCl3的物质的量,进而计算三者物质的量之比;
(2)结合(1)中NaCl、MgCl2、AlCl3的物质的量之比,计算各物质的量的物质的量,再根据m=nM计算出混合物的质量.
解答 解:(1)设Na、Mg、Al三种元素的质量分别23g、16g、9g,则n(NaCl)=n(Na)=$\frac{23g}{23g/mol}$=1mol,
n(MgCl2)=n(Mg)=$\frac{16g}{24g/mol}$=$\frac{2}{3}$mol,
n(AlCl3)=n(Al)=$\frac{9g}{27g/mol}$=$\frac{1}{3}$mol,
故NaCl、MgCl2、AlCl3的物质的量的比为:1mol:$\frac{2}{3}$mol:$\frac{1}{3}$mol=3:2:1,
答:NaCl、MgCl2、AlCl3的物质的量的之比为3:2:1;
(2)设NaCl、MgCl2、AlCl3的物质的量分别为3x、2x、x,则3x+2x×2+x×3=1,解得x=0.1,
则混合物的质量为:58.5g/mol×0.1×3mol+95g/mol×0.1×2mol+133.5g/mol×0.1mol=49.9g,
答:氯原子为1mol时,混合物的质量为49.9g.
点评 本题考查混合物有关计算、物质的量计算,题目难度中等,注意掌握以物质的量为中心的有关计算,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列元素或物质性质的比较中,正确的是( )
| A. | 元素的最高正化合价:N>S | B. | 热稳定性:HCl>HI | ||
| C. | 碱性:Mg(OH)2>NaOH | D. | 酸性:H2SiO3>H2CO3 |
14.依照阿佛加德罗定律,下列叙述错误的是( )
| A. | 同温同压下两种气体的体积之比等于物质的量之比 | |
| B. | 同温同压下两种气体的物质的量之比等于密度之比 | |
| C. | 同温同压下两种气体的摩尔质量之比等于密度之比 | |
| D. | 同温同体积下两种气体的物质的量之比等于压强之比 |
11.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L SO3中原子数目为4NA | |
| B. | 100mL 1mol•L-1的K2CO3溶液中CO32-数目为0.1NA | |
| C. | 5.6g N2与足量H2反应,转移电子数目小于1.2NA | |
| D. | 9.1g苯和立方烷(C8H8)的混合物中原子数目为0.7NA |
20.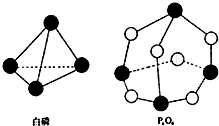 化学反应的本质是旧健的断裂和新键的形成过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的能量变化为( )
化学反应的本质是旧健的断裂和新键的形成过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的能量变化为( )
 化学反应的本质是旧健的断裂和新键的形成过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的能量变化为( )
化学反应的本质是旧健的断裂和新键的形成过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的能量变化为( )| A. | 吸收126kJ的能量 | B. | 释放126kJ的能量 | ||
| C. | 吸收1638kJ的能量 | D. | 释放1638kJ的能量 |
1.如表是A、B、C、D、E五种有机物的有关信息:
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为1,2-二溴乙烷;写出在一定条件下,A生成高分子化合物的化学方程式n CH2=CH2$\stackrel{一定条件}{→}$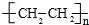 .
.
(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与KMnO4酸性溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式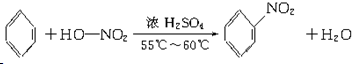 .
.
(4)C与E反应能生成相对分子质量为100的酯,该反应类型为取代反应;其化学方程式为CH2=CHCOOH+CH3CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOOCH2CH3+H2O.
(5)写出由C氧化生成D的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
| A | ①能使溴的四氯化碳溶液褪色; ②能与水在一定条件下反应生成C ③比例模型为:  |
| B | ①由C、H两种元素组成; ②球棍模型为:  |
| C | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与E反应生成相对分子质量为100的酯. |
| D | ①相对分子质量比C少2; ②能由C氧化而成; |
| E | ①由C、H、O三种元素组成; ②球棍模型为: 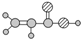 |
(1)A与溴的四氯化碳溶液反应的生成物的名称为1,2-二溴乙烷;写出在一定条件下,A生成高分子化合物的化学方程式n CH2=CH2$\stackrel{一定条件}{→}$
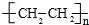 .
.(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与KMnO4酸性溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式
 .
.(4)C与E反应能生成相对分子质量为100的酯,该反应类型为取代反应;其化学方程式为CH2=CHCOOH+CH3CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOOCH2CH3+H2O.
(5)写出由C氧化生成D的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
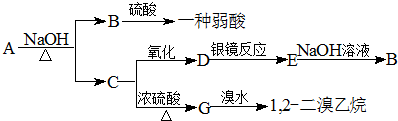
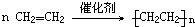 .
.