题目内容
16.下列元素或物质性质的比较中,正确的是( )| A. | 元素的最高正化合价:N>S | B. | 热稳定性:HCl>HI | ||
| C. | 碱性:Mg(OH)2>NaOH | D. | 酸性:H2SiO3>H2CO3 |
分析 A.最外层电子数等于最高正价数;
B.非金属性越强,气态氢化物越稳定;
C.金属性越强,最高价氧化物对应水化物的碱性越强;
D.非金属性越强,最高价氧化物对应水化物的酸性越强.
解答 解:A.N、S的最外层电子数分别为5、6,则元素的最高正化合价:S>N,故A错误;
B.非金属性Cl>I,则氢化物的稳定性为HCl>HI,故B正确;
C.金属性Na>Mg,则碱性:Mg(OH)2<NaOH,故C错误;
D.非金属性C>Si,则酸性:H2SiO3<H2CO3,故D错误;
故选B.
点评 本题考查元素周期律和元素周期表,为高频考点,把握元素的位置、性质及元素周期律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
6.如图是氢氧燃料电池构造示意图.下列说法不正确的是( )
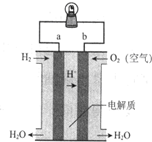

| A. | a极是负极 | B. | 电子由b通过溶液流向a | ||
| C. | 该电池总反应是2H2+O2═H2O | D. | 氢氧燃料电池是环保电池 |
4.保护环境,就是保护人类自己.目前,在我国的城市环境中最主要的大气污染物是( )
| A. | CO2、Br2、Cl2、酸雨 | B. | NH3、CO2、NO2、雾 | ||
| C. | HCl、SO2、N2、粉尘 | D. | SO2、NO2、CO、烟尘 |
11.在一定温度下,向a L密闭容器中加入一定量A、B气体,发生如下反应:A2(g)+3B(g)?2C2 (g)+2D(g),下列叙述能说明该反应达到化学平衡状态的是( )
| A. | 容器中总压强不再随时间而变化 | |
| B. | v正(B)=0.03mol/(L•s),v逆(D)=1.2mol/(L•min) | |
| C. | 单位时间内断裂一个A-A键,同时生成两个C-C键 | |
| D. | 容器中混合气体的密度不再随时间而变化 |
1.下列关于乙烯的说法正确的是( )
| A. | 分子中的6个原子在同一平面上 | |
| B. | 通常状况下,是易溶于水的气体 | |
| C. | 与酸性高锰酸钾溶液的反应是加成反应 | |
| D. | 不能发生燃烧反应和加聚反应 |
8.下列各物质中,存在顺反异构体的是( )
| A. | 1-丁烯 | B. | 丙烯 | C. | 2-氯-2-丁烯 | D. | 2-甲基-2-丁烯 |
5.下列化学用语正确的是( )
| A. | 硅的原子结构示意图: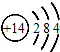 | |
| B. | 原子核内有8个中子的氧原子:${\;}_{8}^{18}$O | |
| C. | 二氧化碳分子的电子式: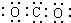 | |
| D. | 甲烷分子的比例模型: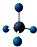 |