题目内容
1.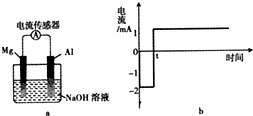 将打磨后的镁和铝平行插入1mol•L-1NaOH溶液中,用导线相连并连接电流传感器组成原电池装置(如图a),测得电流随时间变化曲线如图b所示(起始时镁作负极,t时刻电流出现反转),且镁条表面始终无明显气泡,则下列说法中错误的是( )
将打磨后的镁和铝平行插入1mol•L-1NaOH溶液中,用导线相连并连接电流传感器组成原电池装置(如图a),测得电流随时间变化曲线如图b所示(起始时镁作负极,t时刻电流出现反转),且镁条表面始终无明显气泡,则下列说法中错误的是( )| A. | 实验过程中,铝电极表面可能有气泡产生 | |
| B. | 0-t时刻,镁电极上发生反应:Mg-2e-+2OH-=Mg(OH)2 | |
| C. | t时刻时,铝和镁的金属活动性相同 | |
| D. | t时刻后,电池主要的总反应方程式:4Al+3O2+4OH-=4AlO2-+2H2O |
分析 A、实验过程中,铝电极表面是水电离产生的氢离子放电,生成氢气;
B、0-t时刻,镁作为负极失去电子,生成镁离子,镁离子与氢氧根离子结合生成氢氧化镁:
C、指针未偏转,说明未形成电流;
D、t时刻后,铝是负极发生氧化反应,镁是正极,发生还原反应,水电离产生的氢离子在正极放电.
解答 解:A、起始时镁作负极,铝电极表面是水电离产生的氢离子放电,生成氢气,所以铝电极表面可能有气泡产生,故A正确;
B、0-t时刻,镁作为负极失去电子,生成镁离子,镁离子与氢氧根离子结合生成氢氧化镁,所以电极反应式为:Mg-2e-+2OH-=Mg(OH)2,故B正确:
C、指针未偏转,说明未形成电流,但镁、铝的活动性不同,故C错误;
D、t时刻后,铝是负极发生氧化反应,镁是正极,发生还原反应,水电离产生的氢离子在正极放电,电极反应的总方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故D错误;
故选CD.
点评 本题考查了原电池和电解池原理,正确推断原电池中正负极是解本题关键,难度中等.

练习册系列答案
相关题目
10.生活中的一些问题常涉及化学知识,下列叙述正确的是( )
①使用明矾可软化硬水;
②硫酸钡难溶于水和酸,可做X光透视肠胃的药剂;
③铁制品在干燥的空气中容易生锈;
④医疗中消毒用的酒精是75%的乙醇溶液;
⑤棉花、蚕丝、人造羊毛的主要成分都是纤维素;
⑥福尔马林是混合物,可用来制作生物标本.
①使用明矾可软化硬水;
②硫酸钡难溶于水和酸,可做X光透视肠胃的药剂;
③铁制品在干燥的空气中容易生锈;
④医疗中消毒用的酒精是75%的乙醇溶液;
⑤棉花、蚕丝、人造羊毛的主要成分都是纤维素;
⑥福尔马林是混合物,可用来制作生物标本.
| A. | ①②③ | B. | ②③⑥ | C. | ①③⑤ | D. | ②④⑥ |
9.化学与生产、生活密切相关,下列有关说法正确的是( )
| A. | 葡萄糖注射液能产生丁达尔效应 | |
| B. | 高纯度的硅单质广泛用于制作光导纤维 | |
| C. | 二氧化硫的大量排放是造成光化学烟雾的主要原因 | |
| D. | 汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2 |
6.用下列装置进行相应的实验,能实现预期目的是( )
| A | B | C | D | |
| 装置 |  |  H2(g)+I2(g)?2HI(g) | 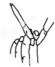 |  |
| 目的 | 检验碳与浓硫酸反应的氧化产物 | 验证压强对化学平衡的影响 | 检查碱式滴定管是否漏液 | FeSO4溶液的蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
13.下列有关实验操作对应的现象及对现象的解释或所得出的结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向浓度均为0.1mol•L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | Ksp(Mg(OH)2)>Ksp(Cu(OH)2) |
| B | 溴乙烷与NaOH溶液共热后,滴加AgNO3溶液 | 未出现淡黄色沉淀 | 溴乙烷未水解 |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中不含K+ |
| D | 某盐溶于盐酸,产生无色无味气体通入澄清石灰水 | 变浑浊 | 说明该盐是碳酸盐 |
| A. | A | B. | B | C. | C | D. | D |
10.25℃时,K甲(BaSO4)=1×10-10,K甲(BaCO3)=2.6×10-8,该温度下,下列说法不正确的是( )
| A. | 相同浓度的Na2SO4和Na2CO3的混合溶液中添加BaCl2溶液,BaSO4先析出 | |
| B. | 向BaCO3的悬浊液中加入少量的新制氯水,r(Ba2+)增大 | |
| C. | BaSO4和BaCO3共存的悬浊液中,c(SO42-)/c(CO32-)=1/26 | |
| D. | 向BaSO4的悬浊液中加入Na2CO3的浓溶液,BaSO4不可能转化为BaCO3 |
 ,合成E和高分子树脂N的路线如图1所示:
,合成E和高分子树脂N的路线如图1所示: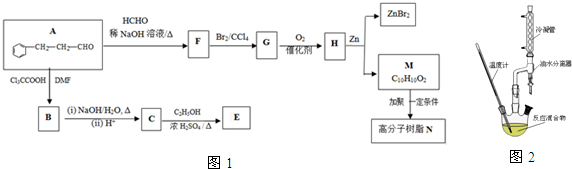
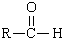 $→_{DMF}^{CI_{3}CCOOH}$
$→_{DMF}^{CI_{3}CCOOH}$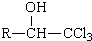 $→_{(ii)H+}^{(i)NaOH/H_{2}O,△}$
$→_{(ii)H+}^{(i)NaOH/H_{2}O,△}$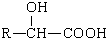
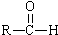 +
+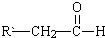 $→_{△}^{稀NaOH溶液}$
$→_{△}^{稀NaOH溶液}$
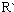 表示烃基或氢原子)
表示烃基或氢原子)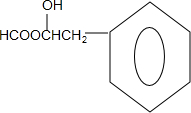
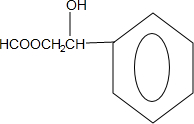 .
.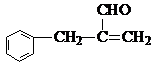 ;N的结构简式为
;N的结构简式为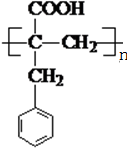 .
.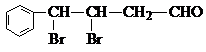 ,下列有关X的说法正确的是ac(填标号).
,下列有关X的说法正确的是ac(填标号).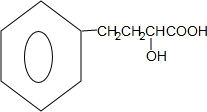 $\stackrel{催化剂}{?}$
$\stackrel{催化剂}{?}$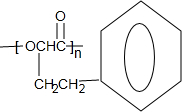 +nH2O.
+nH2O.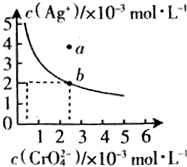 水中的沉淀溶解平衡曲线如图所示. 该温度下.下列说法正确的是AD.
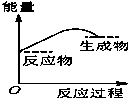
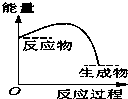
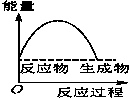
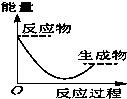
水中的沉淀溶解平衡曲线如图所示. 该温度下.下列说法正确的是AD. 将某固体氢氧化物M与NH4Cl置于如图所示的装置(玻璃片与烧杯底部之间有一薄层水)中混合反应后,用手拿起烧杯时,发现玻璃片与烧杯粘在一起,则该反应所对应的能量变化关系图是( )
将某固体氢氧化物M与NH4Cl置于如图所示的装置(玻璃片与烧杯底部之间有一薄层水)中混合反应后,用手拿起烧杯时,发现玻璃片与烧杯粘在一起,则该反应所对应的能量变化关系图是( )