题目内容
19.在MgCl2、KCl、K2SO4三中盐的混合溶液中,若K+、Cl-、Mg2+的物质的量分别为1.5mol、1.5mol、0.5mol,则SO42-的物质的量为( )| A. | 0.1mol | B. | 0.15mol | C. | 0.5mol | D. | 0.75mol |
分析 混合溶液呈电中性,根据电荷守恒有n(Cl-)+2n(SO42-)=n(K+)+2n(Mg2+),据此计算n(SO42-).
解答 解:混合溶液呈电中性,根据电荷守恒有n(Cl-)+2n(SO42-)=n(K+)+2n(Mg2+),故:
1.5mol+2n(SO42-)=1.5mol+0.5mol×2
解得:n(SO42-)=0.5 mol,
故选C.
点评 本题考查物质的量的有关计算,难度中等,注意电解质混合溶液中离子浓度的计算经常利用电荷守恒进行计算.

练习册系列答案
相关题目
14.2.3g纯净物金属钠在干燥空气中被氧化后得到3.5g固体,由此可判断其氧化产物是( )
| A. | 只有Na2O | B. | 只有Na2O2 | C. | Na2O和Na2O2 | D. | 无法确定 |
4.下列有关物理量相应的单位,表达不正确的是( )
| A. | 摩尔质量:g | B. | 密度:g•mL-1 | ||
| C. | 气体摩尔体积:L•mol-1 | D. | 阿伏加德罗常数:mol-1 |
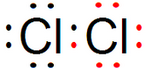 ,比较S2-与Cl-的半径大小:r(S2-)>(填“>”或“<”)r(Cl-).
,比较S2-与Cl-的半径大小:r(S2-)>(填“>”或“<”)r(Cl-). 4-甲基-1-戊烯
4-甲基-1-戊烯 苯甲酸
苯甲酸

 B.
B. 与
与 C.
C. 与
与 D.
D. 与
与 E.
E. 与
与 F.2-甲基丁烷和2,2-二甲基丙烷.
F.2-甲基丁烷和2,2-二甲基丙烷.