题目内容
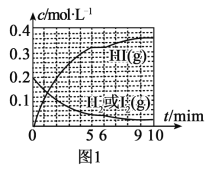
【题目】一定条件下的密闭容器中:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是
4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是
A.向容器中充入4 mol NH3和5 mol O2进行反应,达到平衡时放出的热量为905.9 kJ。
B.平衡时v正(O2)=v逆(NO)。
C.平衡后降低压强,混合气体平均摩尔质量增大。
D.平衡后升高温度,混合气体中NO含量降低。
【答案】D
【解析】
A.该反应为可逆反应,故反应达平衡时反应物不能全部转化为生成物,放出的热量小于905.9 kJ,A项错误;
B.同一反应中,各物质的化学反应速率之比等于化学方程式中相应各物质的化学计量数之比,故![]() ,根据题给信息,则
,根据题给信息,则![]() ,此时
,此时![]() ,说明平衡时
,说明平衡时![]() ,B项错误;
,B项错误;
C.降低压强,平衡右移,气体的总物质的量增大,混合气体的质量不变,故混合气体的平均摩尔质量减小,C项错误;
D.升高温度,平衡向左移动,混合气体中的NO含量降低,D项正确;
答案选D。

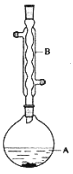
【题目】乙酸异戊酯是组成蜜蜂信息素质的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图和有关数据如下:
![]() +H2O
+H2O
相对原子质量 | 密度/(g.cm-3) | 沸点/℃ | 水中溶解性 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
实验步骤:
在A中加入4.4g的异戊醇,6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50分钟,反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g。回答下列问题:
(1)装置B的名称是:___。
(2)该反应中浓硫酸的作用___,若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式___。
(3)如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作___。
(4)在洗涤操作中,第一次水洗的主要目的是:___;第二次水洗的主要目的是:___。
(5)本实验中加入过量乙酸的目的是:___。
(6)在蒸馏操作中,仪器选择及安装都正确的是:___(填标号)
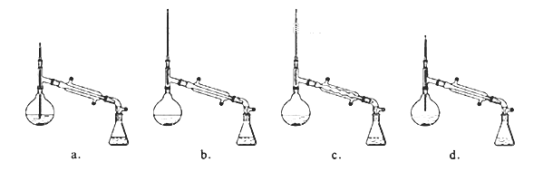
(7)本实验的产率是___。
A.30℅ B.40℅ C.50℅ D.60℅
(8)在进行蒸馏操作时,若从130℃开始收集馏分,产率偏___(填高或者低)原因是___。