题目内容
【题目】实验室需要0.1 mol·L1NaOH溶液500 mL。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,还需要的玻璃仪器是________。
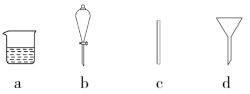
(2)根据计算用托盘天平称取的NaOH固体质量为__________g。
(3)关于容量瓶的四种叙述:
①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是______(填字母)。
A.①②③④ B.②③ C.①②④ D.②③④
(4)容量瓶上需标有以下五项中的_________________(填序号)。
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(5)配制时,其正确的操作顺序是_________(用字母表示,每个操作只用一次)。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(6)下列配制的溶液浓度偏低的是____________(填序号)。
A.称量NaOH时,砝码错放在左盘
B.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C.加蒸馏水时不慎超过了刻度线
D.定容时俯视刻度线
E.配制前,容量瓶中有少量蒸馏水
【答案】bd 胶头滴管和500mL容量瓶 2.0g A ①③⑤ BCAFED BC
【解析】
(1)根据图示可知,配制溶液时用到烧杯和玻璃棒,不会用到有漏斗和分液漏斗,故选bd,还缺少的玻璃仪器是胶头滴管和500mL容量瓶;
(2)500mL 0.1mol·L-1的氢氧化钠溶液,需要NaOH的质量为:40g·mol-1×0.1mol·L-1×0.5L=2.0g;
(3)容量瓶是配制准确的一定物质的量浓度的溶液用的精确仪器。它是一种带有磨口玻璃塞的细长颈、梨形的瓶底玻璃瓶,颈上有刻度;使用时要先检验密闭性,不能在容量瓶里进行溶质的溶解,容量瓶不能进行加热,容量瓶只能用于配制溶液,不能长时间或长期储存溶液;对照4个选项,均正确;
故选A。
(4)容量瓶上需标有以下五项中的①温度③容量⑤刻度线,故选①③⑤;
(5)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶等,所以正确的顺序为:BCAFED;
(6)分析操作对溶质的物质的量和溶液体积的影响,依据c=![]() 进行误差分析。
进行误差分析。
A.称量NaOH时,砝码错放在左盘,当不用游码时,对浓度没有影响,故A不选;
B.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面,导致部分溶质损耗溶质的物质的量偏小,溶液浓度偏低,故B选;
C.加蒸馏水时不慎超过了刻度线,溶液被冲稀,故C选;
D.向容量瓶加水定容时眼睛俯视液面,导致溶液体积偏低,溶液浓度偏高,故D不选;
E.配制前,容量瓶中有少量蒸馏水,定容时要加水,对浓度没有影响,故E不选;
故选BC。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】有七种元素,其中A、X、Y、D、E为短周期主族元素,Z、G为第四周期元素,它们的原子序数依次增大。请回答问题。
A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
X | 元素原子的核外 |
Y | 原子的第一至第四电离能分别是: |
D | 原子核外所有 |
E | 元素的主族序数与周期数的差为4 |
Z | 是前四周期中电负性最小的元素 |
G | 在周期表的第七列 |
(1)已知![]() 为离子化合物,写出其电子式_______________。
为离子化合物,写出其电子式_______________。
(2)X基态原子中能量最高的电子,其电子云在空间有______个方向,原子轨道呈_____形;![]() 的空间构型为__________。
的空间构型为__________。
(3)某同学根据上述信息,推断Y基态原子的核外电子排布为:
![]()
该同学所画的电子排布图违背了________________________。
(4)G位于元素周期表的_________区,原子结构示意图为____________________。
(5)![]() 中心原子的杂化方式为_________,其空间构型为____________________。
中心原子的杂化方式为_________,其空间构型为____________________。
(6)Z元素的基态原子价电子排布式为_______________________。
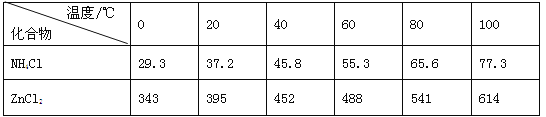
【题目】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,MnO2,ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,有关数据下表所示:
溶解度/(g/100g水)
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的正极反应式为___,电池反应的离子方程式为___。
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn___g。(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过___分离回收;滤渣的主要成分是MnO2、___和_______,欲从中得到较纯的MnO2,最简便的方法是___,其原理是___。