جâؤ؟ؤعبف
،¾جâؤ؟،؟آب»¯راح![]() تاسذ»ْ؛د³ةضذس¦سأ¹م·؛µؤ´ك»¯¼ء،£ثüخ¢بـسعث®£¬²»بـسعزز´¼£¬آ¶ضأسع³±تھµؤ؟صئّضذز×±»رُ»¯£¬µ«شع¸ةشïµؤ؟صئّضذخب¶¨£¬¼û¹â»ل·ض½â،£تµرéتزضئ±¸CuClµؤ¹³جبçدآ£؛
تاسذ»ْ؛د³ةضذس¦سأ¹م·؛µؤ´ك»¯¼ء،£ثüخ¢بـسعث®£¬²»بـسعزز´¼£¬آ¶ضأسع³±تھµؤ؟صئّضذز×±»رُ»¯£¬µ«شع¸ةشïµؤ؟صئّضذخب¶¨£¬¼û¹â»ل·ض½â،£تµرéتزضئ±¸CuClµؤ¹³جبçدآ£؛
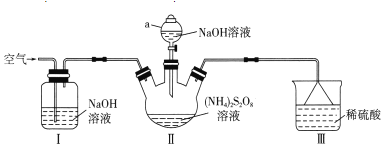
¢ٌ،¢¼ى–ثح¼×°ضأئّأـذش£¬زہ´خدٍب¾±ئ؟ضذ¼سبëحث؟،¢![]() ،¢
،¢![]() ،¢HCl£¬¹ط±صK£»
،¢HCl£¬¹ط±صK£»
¢ٍ،¢¼سببضء![]() ت±ح£ض¹¼سبب£¬حث؟±يأو²ْةْخقة«ئّإف£¬ز؛أوةد·½ئّجهضً½¥±نخھ؛ى×طة«£¬ئّؤز¹ؤئً£»
ت±ح£ض¹¼سبب£¬حث؟±يأو²ْةْخقة«ئّإف£¬ز؛أوةد·½ئّجهضً½¥±نخھ؛ى×طة«£¬ئّؤز¹ؤئً£»
¢َ،¢´ٍ؟ھK£¬ح¨بë![]() £¬´ئّؤز±ن±ٌ،¢ئ؟ؤع؛ى×طة«ئّجهدûت§ت±¹ط±صK£¬ہنب´ضءتزخآ£¬ضئ
£¬´ئّؤز±ن±ٌ،¢ئ؟ؤع؛ى×طة«ئّجهدûت§ت±¹ط±صK£¬ہنب´ضءتزخآ£¬ضئ![]()
¢ô،¢½«ز؛جه×ھزئضءةص±ضذسأ×مء؟صôءَث®د،تح£¬²ْةْ°×ة«³ءµي£¬¹آثµأCuCl´ضئ·؛حآثز؛£»
¢ُ،¢´ضئ·سأ![]() زز´¼د´µس،¢؛و¸ةµأCuCl،£
زز´¼د´µس،¢؛و¸ةµأCuCl،£
اë»ط´ًدآءذختجâ£؛
¢إتµرéتزضذCuC1µؤ±£´و·½·¨تا______
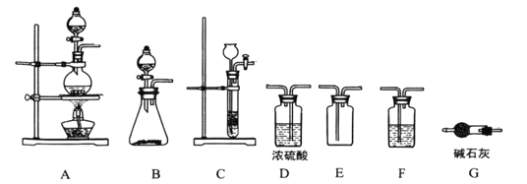
¢ئح¨بë![]() µؤؤ؟µؤتا______£¬خھ±مسع¹غ²ى؛ح؟طضئ²ْةْ
µؤؤ؟µؤتا______£¬خھ±مسع¹غ²ى؛ح؟طضئ²ْةْ![]() µؤثظآت£¬ضئ±¸
µؤثظآت£¬ضئ±¸![]() µؤ×°ضأ×î؛أر،سأ______
µؤ×°ضأ×î؛أر،سأ______![]() جî×ضؤ¸
جî×ضؤ¸![]()

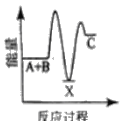
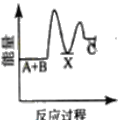
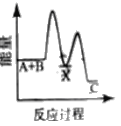
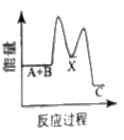
¢ا¢ظب¾±ئ؟ضذةْ³ة![]() µؤ×ـ·´س¦µؤہë×س·½³جت½خھ______
µؤ×ـ·´س¦µؤہë×س·½³جت½خھ______
¢ع²½ضè¢ôضذ²ْةْ°×ة«³ءµيµؤ»¯ر§·½³جت½خھ______
¢ب²½ضèVضذد´µست±تش¼ءر،سأ![]() زز´¼µؤشزٍتا______
زز´¼µؤشزٍتا______
¢ة![]() ´؟¶ب²â¶¨£؛³ئب،رùئ·
´؟¶ب²â¶¨£؛³ئب،رùئ·![]() ضأسعش¤دب·إبë²£ء§ضé30ء£؛ح10mL¹ء؟µؤ
ضأسعش¤دب·إبë²£ء§ضé30ء£؛ح10mL¹ء؟µؤ![]() بـز؛µؤ׶ذخئ؟ضذ£¬²»¶دز،¶¯£»´رùئ·بـ½â؛َ£¬¼سث®50mL؛حض¸ت¾¼ء2µخ£»ء¢¼´سأ
بـز؛µؤ׶ذخئ؟ضذ£¬²»¶دز،¶¯£»´رùئ·بـ½â؛َ£¬¼سث®50mL؛حض¸ت¾¼ء2µخ£»ء¢¼´سأ![]() ءٍثلîو±ê×¼بـز؛µخ¶¨ضءضصµم²¢¼اآ¼¶ءت£¬شظضط¸´تµرéء½´خ£¬²âµأت¾فبç±يثùت¾،£(زرضھ£؛
ءٍثلîو±ê×¼بـز؛µخ¶¨ضءضصµم²¢¼اآ¼¶ءت£¬شظضط¸´تµرéء½´خ£¬²âµأت¾فبç±يثùت¾،£(زرضھ£؛![]() £¬
£¬![]() )
)
تµرéذٍ؛إ | 1 | 2 | 3 |
µخ¶¨ئًت¼¶ءت |
|
|
|
µخ¶¨ضصµم¶ءت |
|
|
|
![]() ²£ء§ضéµؤ×÷سأ______
²£ء§ضéµؤ×÷سأ______
![]() µؤ´؟¶بخھ______
µؤ´؟¶بخھ______![]() ±£ءôبخ»سذذ§ت×ض
±£ءôبخ»سذذ§ت×ض![]() ،£
،£

،¾´ً°¸،؟¸ةشï،¢أـ±صµؤبفئ÷ضذ£¬±ـ¹â±£´و ½«ب¾±ئ؟ضذµؤ![]() ×ھ»¯خھ
×ھ»¯خھ![]() B
B ![]()
![]() ³ب¥CuCl±يأو¸½×إµؤ
³ب¥CuCl±يأو¸½×إµؤ![]() £¬سضؤـر¸ثظ»س·¢´ّ×كCuCl±يأوµؤث®·ف£¬·ہض¹ئن±»رُ»¯ ¼سثظرùئ·بـ½â
£¬سضؤـر¸ثظ»س·¢´ّ×كCuCl±يأوµؤث®·ف£¬·ہض¹ئن±»رُ»¯ ¼سثظرùئ·بـ½â ![]()
،¾½âخِ،؟
¢إسةذإد¢؟ةضھ£¬µأµ½تµرéتزضذCuC1µؤ±£´و·½·¨،£
¢ئ´ٍ؟ھK£¬ح¨بëرُئّ£¬´ئّؤز±ن±ٌ،¢ئ؟ؤع؛ى×طة«ئّجهدûت§£¬ثµأ÷¶رُ»¯µھسëرُئّ،¢ث®×ھ»¯³ة![]() £»¸ù¾فح¼ت¾؟ةضھ£¬B×°ضأ؟ةزش¸ù¾ف׶ذخئ؟ؤعئّإفµؤ؟ىآإذ¶د²ْةْ
£»¸ù¾فح¼ت¾؟ةضھ£¬B×°ضأ؟ةزش¸ù¾ف׶ذخئ؟ؤعئّإفµؤ؟ىآإذ¶د²ْةْ![]() µؤثظآت½ّذذ؟طضئ£¬¶ّA،¢C×°ضأخق·¨إذ¶دح¨بëرُئّµؤثظآت،£
µؤثظآت½ّذذ؟طضئ£¬¶ّA،¢C×°ضأخق·¨إذ¶دح¨بëرُئّµؤثظآت،£
¢ا¢ظحث؟،¢آب»¯°±،¢دُثل،¢رخثل·´س¦ةْ³ة![]() ؛حخقة«ئّإفNO£¬ذ´³ِ·´س¦µؤہë×س·½³جت½،£
؛حخقة«ئّإفNO£¬ذ´³ِ·´س¦µؤہë×س·½³جت½،£
¢ع²½ضè¢ôضذ²ْةْ°×ة«³ءµيµأµ½»¯ر§·½³جت½،£
¢بزٍCuClخ¢بـسعث®£¬²ةسأ![]() زز´¼د´µس£¬¼ب³ب¥CuCl±يأو¸½×إµؤ
زز´¼د´µس£¬¼ب³ب¥CuCl±يأو¸½×إµؤ![]() £¬سضؤـر¸ثظ»س·¢´ّ×كCuCl±يأوµؤث®·ف£¬·ہض¹ئن±»رُ»¯،£
£¬سضؤـر¸ثظ»س·¢´ّ×كCuCl±يأوµؤث®·ف£¬·ہض¹ئن±»رُ»¯،£
¢ب¢ظ²£ء§ضéµؤ×÷سأخھ¼سثظرùئ·بـ½â،£
¢ع¼ئثم³ِدû؛ؤµأئ½¾ùضµ£¬شظ¸ù¾ف¹طدµت½½¨ء¢µبت½½ّذذ¼ئثم،£
¢إسةذإد¢؟ةضھ£¬تµرéتزضذCuC1µؤ±£´و·½·¨تا¸ةشï،¢أـ±صµؤبفئ÷ضذ£¬±ـ¹â±£´و£»¹ت´ً°¸خھ£؛¸ةشï،¢أـ±صµؤبفئ÷ضذ£¬±ـ¹â±£´و،£
¢ئ´ٍ؟ھK£¬ح¨بëرُئّ£¬´ئّؤز±ن±ٌ،¢ئ؟ؤع؛ى×طة«ئّجهدûت§£¬ثµأ÷¶رُ»¯µھسëرُئّ،¢ث®×ھ»¯³ة![]() £¬¹تح¨بëرُئّµؤؤ؟µؤتاخھءث½«ب¾±ئ؟ضذµؤ
£¬¹تح¨بëرُئّµؤؤ؟µؤتاخھءث½«ب¾±ئ؟ضذµؤ![]() ·´س¦ةْ³ة
·´س¦ةْ³ة![]() £»¸ù¾فح¼ت¾؟ةضھ£¬B×°ضأ؟ةزش¸ù¾ف׶ذخئ؟ؤعئّإفµؤ؟ىآإذ¶د²ْةْ
£»¸ù¾فح¼ت¾؟ةضھ£¬B×°ضأ؟ةزش¸ù¾ف׶ذخئ؟ؤعئّإفµؤ؟ىآإذ¶د²ْةْ![]() µؤثظآت½ّذذ؟طضئ£¬¶ّA،¢C×°ضأخق·¨إذ¶دح¨بëرُئّµؤثظآت£¬¹تر،شٌB×°ضأ£»¹ت´ً°¸خھ£؛½«ب¾±ئ؟ضذµؤ
µؤثظآت½ّذذ؟طضئ£¬¶ّA،¢C×°ضأخق·¨إذ¶دح¨بëرُئّµؤثظآت£¬¹تر،شٌB×°ضأ£»¹ت´ً°¸خھ£؛½«ب¾±ئ؟ضذµؤ![]() ×ھ»¯خھ
×ھ»¯خھ![]() £» B،£
£» B،£
¢ا¢ظحث؟،¢آب»¯°±،¢دُثل،¢رخثل·´س¦ةْ³ة![]() ؛حخقة«ئّإفNO£¬¸أ·´س¦µؤہë×س·½³جت½خھ
؛حخقة«ئّإفNO£¬¸أ·´س¦µؤہë×س·½³جت½خھ![]() £»¹ت´ً°¸خھ£؛
£»¹ت´ً°¸خھ£؛![]() ،£
،£
¢ع²½ضè¢ôضذ²ْةْ°×ة«³ءµيµؤ»¯ر§·½³جت½خھ![]() £»¹ت´ً°¸خھ£؛
£»¹ت´ً°¸خھ£؛![]() ،£
،£
¢بزٍCuClخ¢بـسعث®£¬²ةسأ![]() زز´¼د´µس£¬¼ب³ب¥CuCl±يأو¸½×إµؤ
زز´¼د´µس£¬¼ب³ب¥CuCl±يأو¸½×إµؤ![]() £¬سضؤـر¸ثظ»س·¢´ّ×كCuCl±يأوµؤث®·ف£¬·ہض¹ئن±»رُ»¯£»¹ت´ً°¸خھ£؛¼ب³ب¥CuCl±يأو¸½×إµؤ
£¬سضؤـر¸ثظ»س·¢´ّ×كCuCl±يأوµؤث®·ف£¬·ہض¹ئن±»رُ»¯£»¹ت´ً°¸خھ£؛¼ب³ب¥CuCl±يأو¸½×إµؤ![]() £¬سضؤـر¸ثظ»س·¢´ّ×كCuCl±يأوµؤث®·ف£¬·ہض¹ئن±»رُ»¯،£
£¬سضؤـر¸ثظ»س·¢´ّ×كCuCl±يأوµؤث®·ف£¬·ہض¹ئن±»رُ»¯،£
¢ب¢ظ²£ء§ضéµؤ×÷سأخھ¼سثظرùئ·بـ½â£¬¹ت´ً°¸خھ£؛¼سثظرùئ·بـ½â،£
¢عسة![]() ،¢
،¢![]() ؟ةضھ£¬´وشع
؟ةضھ£¬´وشع![]() £¬تµرé1،¢2،¢3دû؛ؤ±ê×¼ز؛جه»·ض±ًخھ
£¬تµرé1،¢2،¢3دû؛ؤ±ê×¼ز؛جه»·ض±ًخھ![]() ،¢
،¢![]() ،¢
،¢![]() £¬µعز»×éت¾فخَ²î½د´َ£¬س¦ةلب¥£¬شٍدû؛ؤµؤ±ê×¼ز؛µؤئ½¾ùجه»خھ
£¬µعز»×éت¾فخَ²î½د´َ£¬س¦ةلب¥£¬شٍدû؛ؤµؤ±ê×¼ز؛µؤئ½¾ùجه»خھ![]() £¬¸ù¾ف
£¬¸ù¾ف![]() ،¢
،¢![]() ؟ةµأ¹طدµت½
؟ةµأ¹طدµت½![]() £¬شٍ
£¬شٍ![]() £¬ثùزشCuClµؤ´؟¶بخھ
£¬ثùزشCuClµؤ´؟¶بخھ![]() £»¹ت´ً°¸خھ£؛
£»¹ت´ً°¸خھ£؛![]() ،£
،£

،¾جâؤ؟،؟¹¤زµةدضئب،CuCl2µؤةْ²ْء÷³جبçدآ£؛

اë½ل؛ددآ±يت¾ف£¬»ط´ًختجâ£؛
خïضت | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
بـ¶ب»(25 ،و) | 8.0،ء10-16 | 2.2،ء10-20 | 4.0،ء10-38 |
حêب«³ءµيت±µؤpH·¶خ§ | ،ف9.6 | ،ف6.4 | 3~4 |
(1)شعبـز؛Aضذ¼سبëNaClOµؤؤ؟µؤتا_________________،£
(2)شعبـز؛Bضذ¼سبëCuOض÷زھةو¼°µؤہë×س·´س¦·½³جت½خھ________________،£
(3)²ظ×÷aخھ___________،£
(4)شعCu(OH)2ضذ¼سبëرخثلت¹Cu(OH)2×ھ»¯خھCuCl2£¬²ةسأةش¹ء؟رخثل؛حµحخآصô¸ةµؤؤ؟µؤتا___،£
،¾جâؤ؟،؟ہàحئث¼خ¬تا»¯ر§½âجâضذ³£سأµؤز»ضضث¼خ¬·½·¨£¬دآءذسذ¹ط·´س¦·½³جت½£¨»ٍہë×س·½³جت½£©µؤہàحئصب·µؤتا£¨،،،،£©
زرضھ | ہàحئ | |
A | ½«Fe¼سبëCuSO4بـز؛ضذ£؛ Fe + Cu2+ = Cu + Fe2+ | ½«Na¼سبëµ½CuSO4بـز؛ضذ£؛ 2Na + Cu2+ = Cu + 2Na+ |
B | د،ءٍثلسëBa(OH)2بـز؛·´س¦ضءبـز؛³تضذذش£؛ 2H++SO42©پ+Ba2++2OH©پ=BaSO4،+2H2O | NaHSO4بـز؛سëBa(OH)2بـز؛·´س¦³تضذذش£؛ 2H++SO42©پ+Ba++2OH©پ=BaSO4،+2H2O |
C | جْ؛حآبئّ·´س¦2Fe+3Cl2 | جْ؛حµ¥ضت·´س¦2Fe+3I2 |
D | دٍCa£¨ClO£©2بـز؛ضذح¨بëةظء؟CO2£؛ Ca2++2ClO©پ+CO2+H2O=CaCO3،+2HClO | دٍCa£¨ClO£©2بـز؛ضذح¨بëةظء؟SO2£؛ Ca2++2ClO©پ+SO2+H2O=CaSO3،+2HClO |
A.AB.BC.CD.D