题目内容
2.下列说法正确的是( )| A. | 钠原子与氯气分子反应生成氯化钠后,其结构的稳定性增强 | |
| B. | 选择燃料只要考虑燃料燃烧值的大小 | |
| C. | 失电子难的原子获得电子的能力一定强 | |
| D. | 两个原子之间的相互作用叫化学键 |
分析 A.化学反应的实质就是旧键断裂新键形成,钠和氯气反应生成氯化钠的反应是放热反应,生成物能量降低,物质能量越高越活泼;
B.选择燃料除考虑热值外,还要考虑污染、制取等等因素;
C.根据原子得失电子的难易与其最外层电子的关系分析;
D.化学键通常指的是相邻的两个或多个原子间的强烈的相互作用.
解答 解:A.化学反应的实质就是旧化学键的断裂,新化学键的形成,物质能量越高越活泼,钠和氯气反应生成氯化钠的反应是放热反应,生成物能量降低,故A正确;
B.选择燃料除考虑热值外,还要考虑污染程度、制取难易等等因素,故B错误;
C.失电子难的原子获得电子的能力不一定强,如稀有气体的原子,故C错误;
D.化学键通常指的是相邻的两个或多个原子间的强烈的相互作用,故D错误.
故选A.
点评 本题考查化学键的概念、燃料的选择、能量变化的原因等,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
10.一定温度下,体积为1L的密闭容器中X、Y、Z三种气体的初始物质的量和平衡物质的量如下表所示:
下列说法正确的是( )
| 物质 | X | Y | Z |
| 初始物质的量(mol) | 0.2 | 0.4 | 0 |
| 平衡物质的量(mol) | 0.1 | 0.1 | 0.2 |
| A. | 反应可表示为X+3Y?2Z,其平衡常数为400 | |
| B. | 向该容器中再加入0.1mol X、0.1mol Y、0.2mol Z,平衡不移动 | |
| C. | 若向容器中再加入0.1mol X,因平衡向右移动,则X、Y、Z的转化率均增大 | |
| D. | 若升高温度时,Z的浓度增大,则容器内的压强增大 |
7.下列有关中和热的说法正确的是( )
| A. | 中和热的热化学方程式:H+(l)+OH-(l)═H2O(l)△H=-57.3 kJ/mol | |
| B. | 准确测量中和热的实验过程中,至少需测定温度4次 | |
| C. | 环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小 | |
| D. | 若稀酸溶液中H+与稀碱溶液中OH-的物质的量相等,则所测中和热数值更准确 |
14.在恒温条件下,向CH3COONa稀溶液中分别加入少量下列物质:其中可使比值$\frac{c(C{H}_{3}CO{O}^{-})}{c(N{a}^{+})}$增大的是( )
| A. | 固体NaOH | B. | 固体KOH | ||
| C. | 相同浓度的 CH3COONa稀溶液 | D. | 氯化钠固体 |
11.下列分子结构中,各原子的最外层电子不能满足8电子稳定结构的是( )
| A. | CO2 | B. | PCl5 | C. | CCl4 | D. | PCl3 |
12.下列实验操作错误的是( )
| A. | 欲除去溴水中混有的少量碘,加入苯进行萃取 | |
| B. | 除去碳酸钠中的少量碳酸氢钠,加热固体 | |
| C. | 除去CO2中的少量SO2:通过盛有足量NaHCO3溶液的洗气瓶 | |
| D. | 提取溶解在水中的少量碘:加入CCl4,振荡、静置、分层后取出有机层再分离 |
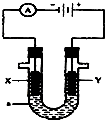 如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: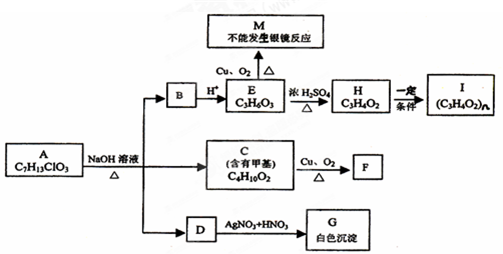
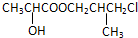 、
、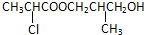
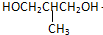 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$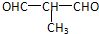 +2H2O;
+2H2O;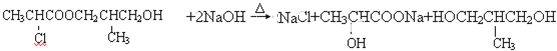 ;
;