题目内容
14.在恒温条件下,向CH3COONa稀溶液中分别加入少量下列物质:其中可使比值$\frac{c(C{H}_{3}CO{O}^{-})}{c(N{a}^{+})}$增大的是( )| A. | 固体NaOH | B. | 固体KOH | ||
| C. | 相同浓度的 CH3COONa稀溶液 | D. | 氯化钠固体 |
分析 醋酸钠溶液中存在醋酸根离子水解平衡:CH3COO-+H2O?CH3COOH+OH-,使$\frac{c(C{H}_{3}CO{O}^{-})}{c(N{a}^{+})}$比值增大,可使平衡向逆反应方向移动,结合影响水解平衡移动的因素解答该题.
解答 解:A、加入固体NaOH,c(Na+)与c(CH3COO-)都增大,但c(Na+)增大幅度较大,则比值减小,故A错误;
B、加入固体KOH,抑制水解,则c(CH3COO-)增大,而c(Na+)不变,则比值增大,故B正确;
C、加入相同浓度的 CH3COONa稀溶液,平衡不移动,则比值不变,故C错误;
D、加入固体NaCl,平衡不移动,但c(Na+)增大,则比值减小,故D错误.
故选B.
点评 本题考查学生盐的水解原理以及影响盐的水解平衡移动等方面的知识,侧重于学生的分析能力的考查,注意知识的归纳整理是解题关键,难度不大.

练习册系列答案
相关题目
4.将一小粒钠投入氯化铁溶液中,反应停止后,观察现象是( )
| A. | 有红褐色沉淀 | B. | 有红褐色沉淀和气体产生 | ||
| C. | 有气体产生,无沉淀生成 | D. | 无沉淀和有气体产生 |
5.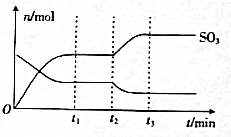 工业生产硫酸的一个重要反应为为2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1.如图表示反应在t1时达到平衡,t2时改变条件,在t3时又重新达到平衡,t2时改变的条件(假设只改变一个条件,其他条件不变)可以是( )
工业生产硫酸的一个重要反应为为2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1.如图表示反应在t1时达到平衡,t2时改变条件,在t3时又重新达到平衡,t2时改变的条件(假设只改变一个条件,其他条件不变)可以是( )
 工业生产硫酸的一个重要反应为为2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1.如图表示反应在t1时达到平衡,t2时改变条件,在t3时又重新达到平衡,t2时改变的条件(假设只改变一个条件,其他条件不变)可以是( )
工业生产硫酸的一个重要反应为为2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1.如图表示反应在t1时达到平衡,t2时改变条件,在t3时又重新达到平衡,t2时改变的条件(假设只改变一个条件,其他条件不变)可以是( )| A. | 减小压强 | B. | 升高反应体系温度 | ||
| C. | 使用新型催化剂 | D. | 加入SO2 |
2.下列说法正确的是( )
| A. | 钠原子与氯气分子反应生成氯化钠后,其结构的稳定性增强 | |
| B. | 选择燃料只要考虑燃料燃烧值的大小 | |
| C. | 失电子难的原子获得电子的能力一定强 | |
| D. | 两个原子之间的相互作用叫化学键 |
9.已知31g白磷变成红磷放出18.39kJ热量,下列两反应中:
P4(s)+5O2(g)═2P2O5(s)△H=Q1 kJ•mol-1
4P(红,s)+5O2(g)═2P2O5(s)△H=Q2kJ•mol-1
则下列说法中正确的是( )
P4(s)+5O2(g)═2P2O5(s)△H=Q1 kJ•mol-1
4P(红,s)+5O2(g)═2P2O5(s)△H=Q2kJ•mol-1
则下列说法中正确的是( )
| A. | Q1>Q2,白磷比红磷稳定 | B. | Q1>Q2,红磷比白磷稳定 | ||
| C. | Q1<Q2,白磷比红磷稳定 | D. | Q1<Q2,红磷比白磷稳定 |
19.用干燥的烧瓶收集氨气做喷泉实验,结果发现进入烧瓶的水占烧瓶总体积的$\frac{2}{3}$,则所收集的气体对空气(相对质量为29)的相对密度约为( )
| A. | 0.59 | B. | 0.72 | C. | 0.84 | D. | 0.91 |
6.N2O俗称“笑气”,曾用作可吸入性麻醉剂,产生N2O反应:3CO+2NO2═3CO2+N2O.下列说法正确的是( )
| A. | 反应中每生成l mol N2O,转移4mol电子 | |
| B. | N2O只有氧化性,无还原性 | |
| C. | N2O和CO2互为等电子体 | |
| D. | NO2属于酸性氧化物 |
3.下列说法正确的是( )
| A. | 离子化合物中一定含有金属元素 | |
| B. | 1mol Na2O2 含有共价键的数目是NA(NA为阿伏加德罗常数) | |
| C. | H2Se比H2O稳定 | |
| D. | Na2O2与H2O反应的过程中,同时有离子键、非极性键的断裂和形成 |