题目内容
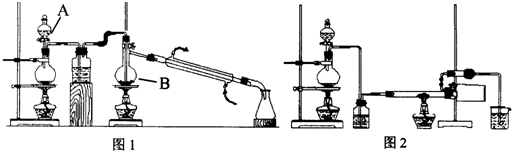
14.实验室制备1-溴丁烷的原理为CH3CH2CH2CH2OH+NaBr+H2SO4$\stackrel{△}{→}$CH3CH2CH2CH2Br+NaHSO4+H2O,根据原理设计实验装置如图1所示.
(1)仪器D的名称为,A处玻璃棒搅拌的目的是使反应物混合均匀并充分反应,提高反应速率.
(2)1-溴丁烷的制备反应中可能有:丁醚、1-丁烷、溴化氢等副产物生成.熄灭A处酒精灯,打开a,余热会使反应继续进行.B、C装置可检验部分副产物,则判断B、C中应盛放的试剂分别是硝酸银溶液或紫色石蕊试液、溴水或酸性高锰酸钾溶液.
(3)为了精制1-溴丁烷,待烧瓶冷却后,将A装置上的玻璃棒换成温度计,关闭a,打开b,使冷水从d(填“c”或“d”)处流入,粗产品蒸馏提纯时,图2 装置中温度计位置正确的是D(填字母,下同),可能会导致收集到的产品中混有低沸点杂质的装置是AB.
(4)称取干燥、纯净的白色不容物7.36g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中,实验后装置A增重0.72g,装置B增重2.64g.白色不容物的化学式为2Mg(OH)2•3MgCO3或Mg5(OH)4(CO3)3.
(5)写出镁与饱和碳酸氢钠溶液反应的化学方程式:5Mg+6NaHCO3+4H2O=2Mg(OH)2•3MgCO3↓+3Na2CO3+5H2↑.
Ⅲ.反应原理分析
(6)NaHCO3 溶液中存在如下电离平衡:H2O?H++OH-、HCO3-?H++CO32-,从平衡移动角度分析实验①产生大量气泡和白色不容物的原因:Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物2Mg(OH)2•3MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行,实验Mg和饱和碳酸氢钠溶液产生大量气体和白色不溶物.
分析 (1)根据装置图可知仪器的名称,三颈烧瓶中反应物要充分混合,需要用玻璃棒搅拌,同时搅拌可加快反应速率;
(2)CH3CH2CH2CH2OH在浓硫酸条件下加热可以生成1-丁烯或丁醚等,图1中B、C可分别用来检验反应产生的气态产物溴化氢、1-丁烯等;
(3)根据冷却时采用逆流,冷却效果较好判断,蒸馏是温度计的水银球位置应与蒸馏烧瓶支管口平齐,如果低于蒸馏烧瓶支管口,则会收集到低沸点的物质;
(4)根据B中碱石灰质量的增加量就是生成的二氧化碳的质量,根据二氧化碳的质量计算出碳酸镁的质量,剩余的就是氢氧化镁的质量,据此计算出白色不溶物的化学式;
(5)根据分析、计算可知,镁与碳酸氢钠溶液反应生成2Mg(OH)2•3MgCO3、碳酸钠和氢气,据此写出反应的化学方程式;
(6)依据碳酸氢钠溶液中存在碳酸氢根离子电离和水的电离平衡,镁和氢离子反应促进电离平衡正向进行,镁离子和氢氧根离子和碳酸根离子形成沉淀分析.
解答 解:(1)根据装置图可知仪器D为直形冷凝管,三颈烧瓶中反应物要充分混合,需要用玻璃棒搅拌,同时搅拌可加快反应速率,所以玻璃棒的作用为使反应物混合均匀并充分反应,提高反应速率,
故答案为:直形冷凝管;使反应物混合均匀并充分反应,提高反应速率;
(2)CH3CH2CH2CH2OH在浓硫酸条件下加热可以生成1-丁烯或丁醚等,所以可能有的杂质为丁醚等,图1中B、C可分别用来检验反应产生的气态产物溴化氢、1-丁烯,B中装硝酸银溶液或紫色石蕊试液用来检验溴化氢,C装置中装入溴水或酸性高锰酸钾溶液用来检验1-丁烯,
故答案为:丁醚;硝酸银溶液或紫色石蕊试液;溴水或酸性高锰酸钾溶液;
(3)根据冷却时采用逆流,冷却效果较好,所以冷水应从d处流入,蒸馏是温度计的水银球位置应与蒸馏烧瓶支管口平齐,所以D装置正确,如果低于蒸馏烧瓶支管口,则会收集到低沸点的物质,所以AB装置符合题意,
故答案为:d;D;AB;
(4)B中碱石灰质量的增加量就是生成的二氧化碳的质量,所以生成二氧化碳的质量为2.64g,设碳酸镁的质量为x,则:
MgCO3+2HCl═MgCl2+H2O+CO2↑
84 44
x 2.64g
x=$\frac{2.64g×84}{44}$=5.04g,
所以氢氧化镁的质量为:7.36g-5.04g=2.32g,
氢氧化镁与碳酸镁的物质的量之比为:$\frac{2.32g}{58g/mol}$:$\frac{5.04g}{84g/mol}$=0.4mol:0.6mol=2:3,
则白色不溶物的化学式为:2Mg(OH)2•3MgCO3或Mg5(OH)4(CO3)3,
故答案为:2Mg(OH)2•3MgCO3或Mg5(OH)4(CO3)3;
(5)根据以上分析可知,镁与饱和碳酸氢钠溶液反应生成2Mg(OH)2•3MgCO3沉淀、Na2CO3和H2,反应的化学方程式为:5Mg+6NaHCO3+4H2O=2Mg(OH)2•3MgCO3↓+3Na2CO3+5H2↑,
故答案为:5Mg+6NaHCO3+4H2O=2Mg(OH)2•3MgCO3↓+3Na2CO3+5H2↑;
(6)NaHCO3溶液中存在平衡,HCO3-?H++CO32-、H2O?H++OH-,Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)2•2MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行,
故答案为:Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物2Mg(OH)2•3MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行,实验Mg和饱和碳酸氢钠溶液产生大量气体和白色不溶物.
点评 本题考查了探究物质组成、测量物质的含量的方法,题目难度较大,试题涉及的内容较多、综合性较强,注意掌握探究物质组成、测量物质含量的方法,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

 特高级教师点拨系列答案
特高级教师点拨系列答案
回答下列问题:
(1)a仪器的名称是分液漏斗
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式2NaNO2+(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O
(3)装置B的作用是除去氧气(及氮氧化物),装置C的作用是除去水蒸气;
(4)已知氮化硅的化学性质稳定,但常温下易溶于氢氟酸溶液生成一种白色的胶状沉淀和一种盐,请写出此化学反应方程式:Si3N4+4HF+9H2O=3H2SiO3↓+4NH4F;
(5)实验室中某些气体的制取、收集及尾气处理装置如右图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是D
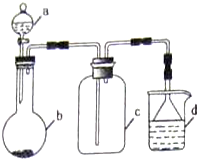
| 选项 | a物质 | b物质 | c收集的气体 | d中的物质 |
| A | 浓氨水 | NaOH | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | 澄清石灰水 |
| C | 稀硝酸 | Fe | NO2 | H2O |
| D | 浓盐酸 | KMnO4 | Cl2 | NaOH溶液 |
| A. | 2.2×10-10 mol/L | B. | 2.2×10-12 mol/L | C. | 2.2×10-14 mol/L | D. | 1.1×10-21 mol/L |
| A. | Fe2+ K+ S${O}_{4}^{2-}$ N${O}_{3}^{-}$ | B. | Mg2+ N${H}_{4}^{+}$ S${O}_{4}^{2-}$ Cl- | ||
| C. | Na+ K+ S${O}_{4}^{2-}$ N${O}_{3}^{-}$ | D. | Ba2+ Na+ Mn${O}_{4}^{-}$ S${O}_{4}^{2-}$ |
| A. | 石油分馏时把温度计插入液面以下 | B. | 可用裂化汽油萃取溴水中的溴 | ||
| C. | 将乙醇加入银氨溶液中加热制银镜 | D. | 将苯和液溴混合后加入Fe粉制溴苯 |
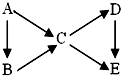 A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系:
A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系: