��Ŀ����
12��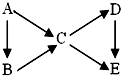 AΪ���ʣ�B��C��D��EΪ��A������ͬԪ�صĻ��������֮��������ת����ϵ��
AΪ���ʣ�B��C��D��EΪ��A������ͬԪ�صĻ��������֮��������ת����ϵ����1����ͼ��B��C��Ϊ�����D��E��Ϊ�Σ���A�����Ǣۣ�������ţ�
��Na ��N2 ��C ��S
��2�����������ʵ���ɫ��Ӧ��Ϊ��ɫ������C��D��E��ˮ��Һ���Լ��ԣ��ҵ�Ũ��ʱ����C��D��E��B������������
��B�к��еĻ�ѧ������Ϊ���Ӽ����Ǽ��Լ�������Ӽ����������Լ����Ǽ��Լ�������
��Bת����C�����ӷ���ʽΪ��2Na2O2+2H2O=4Na++4OH-+O2��
��Dת����E�����ӷ���ʽΪ��CO32-+CO2+H2O=2HCO3-��
��3����������B��C��D��Ϊ���壬��DΪ����ɫ���壮
��д��B��C�Ļ�ѧ����ʽΪ4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
�ڽ�B��CO2����ͨ�뱥��ʳ��ˮ����̼�����ƾ�����������Ӧ�����ӷ���ʽ�ǣ�NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3��
��4����CΪdz��ɫ��Һ��BΪ��ɫ��Һ��EΪ���ɫ������д��Dת����E�Ļ�ѧ����ʽ��4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
���� AΪ���ʣ�B��C��D��EΪ��A������ͬԪ�صĻ����
��1����ͼ��B��C��Ϊ�����D��E��Ϊ�Σ�A��ֱ������CҲ��ֱ������B���������ѡ���Aֻ����Na��C����A��Na����BΪNa2O��CΪNa2O2��C����DҲ������E����D��E����Ϊ�������ƺ�̼���ƣ������Ͼ�Ϊ�Σ�����A��C��BΪCO��CΪCO2��C����DҲ������E����D����E������EΪ̼���ơ�DΪ̼�����ƣ���DΪ̼���ơ�EΪ̼�����ƣ�������ת����ϵ��
��2�����������ʵ���ɫ��Ӧ��Ϊ��ɫ��˵����������Ԫ�أ���AΪNa��B��������������BΪNa2O2������C��D��E��ˮ��Һ���Լ��ԣ��ҵ�Ũ��ʱ����C��D��E����CΪNaOH��DΪNa2CO3��EΪNaHCO3��
��3����������B��C��D��Ϊ���壬��DΪ����ɫ���壬����DΪNO2������AΪN2������ͼ��ת����ϵ��B��CO2����ͨ�뱥��ʳ��ˮ����̼�����ƾ���������BΪNH3��CΪNO��EΪHNO3��
��4��EΪ���ɫ��������EΪFe��OH��3������ͼ��ת����ϵ��AΪFe��CΪdz��ɫ��Һ����CΪFeCl2��BΪ��ɫ��Һ����BΪFeCl3��DΪFe��OH��2���ݴ˴��⣮
��� �⣺AΪ���ʣ�B��C��D��EΪ��A������ͬԪ�صĻ����
��1����ͼ��B��C��Ϊ�����D��E��Ϊ�Σ�A��ֱ������CҲ��ֱ������B���������ѡ���Aֻ����Na��C����A��Na����BΪNa2O��CΪNa2O2��C����DҲ������E����D��E����Ϊ�������ƺ�̼���ƣ������Ͼ�Ϊ�Σ�����A��C��BΪCO��CΪCO2��C����DҲ������E����D����E������EΪ̼���ơ�DΪ̼�����ƣ���DΪ̼���ơ�EΪ̼�����ƣ�������ת����ϵ������A��C��
�ʴ�Ϊ���ۣ�
��2�����������ʵ���ɫ��Ӧ��Ϊ��ɫ��˵����������Ԫ�أ���AΪNa��B��������������BΪNa2O2������C��D��E��ˮ��Һ���Լ��ԣ��ҵ�Ũ��ʱ����C��D��E����CΪNaOH��DΪNa2CO3��EΪNaHCO3��
��BΪNa2O2��B�к��еĻ�ѧ������Ϊ���Ӽ����Ǽ��Լ����ʴ�Ϊ�����Ӽ����Ǽ��Լ���
��Na2O2ת����NaOH�����ӷ���ʽΪ��2Na2O2+2H2O=4Na++4OH-+O2�����ʴ�Ϊ��2Na2O2+2H2O=4Na++4OH-+O2����
��Na2CO3ת����NaHCO3�����ӷ���ʽΪCO32-+CO2+H2O=2HCO3-���ʴ�Ϊ��CO32-+CO2+H2O=2HCO3-��
��3����������B��C��D��Ϊ���壬��DΪ����ɫ���壬����DΪNO2������AΪN2������ͼ��ת����ϵ��B��CO2����ͨ�뱥��ʳ��ˮ����̼�����ƾ���������BΪNH3��CΪNO��EΪHNO3��
��д��B��C�Ļ�ѧ����ʽΪ 4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O���ʴ�Ϊ��4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
�ڽ�B��CO2����ͨ�뱥��ʳ��ˮ����̼�����ƾ�����������Ӧ�����ӷ���ʽ��NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3���ʴ�Ϊ��NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3��
��4��EΪ���ɫ��������EΪFe��OH��3������ͼ��ת����ϵ��AΪFe��CΪdz��ɫ��Һ����CΪFeCl2��BΪ��ɫ��Һ����BΪFeCl3��DΪFe��OH��2��Dת����E�Ļ�ѧ����ʽ4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
�ʴ�Ϊ��4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
���� ���⿼��������ƶϣ�ע��������Ϣ��ת����ϵͼ�ƶϸ������ǽ��Ĺؼ���ϰ���ۺ��Խ�ǿ���漰�Ȼ�ѧ��Ӧ�����ӷ�Ӧ����Һ�������غ㡢����غ�Ŀ��飬��Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | ��ϩ���ӵı���ģ��ʾ��ͼ�� | B�� | �Ҵ��ķ���ʽ��CH3CH2OH | ||
| C�� | 2-��-2-��ϩ�ļ���ʽ��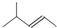 | D�� | ����Na+[��$\underset{\stackrel{..}{S}}{..}$��]2Na+ |
| A�� | 78% | B�� | 22% | C�� | 14% | D�� | 13% |
| ������ | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Ԫ���� | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
��2�����ڱ��еڢ�B������Ԫ����࣬�ڢ�A��Ԫ���γɻ�����������࣮
��3���������������Ԫ�����Ĺ�ϵ��Ԥ�Ե�8���������ܺ���Ԫ������ΪC��
A��18 B��32 C��50 D��64��
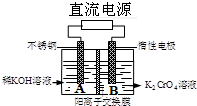 ��ͼ��ʾ�䷴Ӧԭ�����Ա�ʾΪ4K2CrO4+4H2O$\frac{\underline{\;���\;}}{\;}$ 2K2Cr2O7+4KOH+2H2��+O2������˵����ȷ���ǣ�������
��ͼ��ʾ�䷴Ӧԭ�����Ա�ʾΪ4K2CrO4+4H2O$\frac{\underline{\;���\;}}{\;}$ 2K2Cr2O7+4KOH+2H2��+O2������˵����ȷ���ǣ�������| A�� | ���ŷ�Ӧ���У�����PH��С | |
| B�� | OH-ͨ����Ĥ����B�� | |
| C�� | B�ص缫������ӦΪ2H2O+4e-4�TH++O2�� | |
| D�� | ÿת��2mol��������2g H2 |
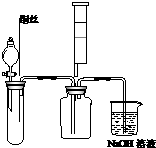 ��1��ijͬѧΪ��֤�����۲쵽ͭ��ϡ���ᷴӦ�IJ���NO��ʵ��ʱ��������ͼ�Թ��м���һ�����Ŀ�״���壬�ٵμӹ�����ϡ���ᣬ����Ӧ��������������Թܺ��ٽ�ͭ˿����ϡ������Һ�У�����Ϊ�Թ��еĿ�״������̼��ƣ��������Ǹ����Թ��еĿ�����ʵ�����ʱ����ע�������Թ����������������������Ŀ���Ǽ���NO���۲쵽����ɫ���壮
��1��ijͬѧΪ��֤�����۲쵽ͭ��ϡ���ᷴӦ�IJ���NO��ʵ��ʱ��������ͼ�Թ��м���һ�����Ŀ�״���壬�ٵμӹ�����ϡ���ᣬ����Ӧ��������������Թܺ��ٽ�ͭ˿����ϡ������Һ�У�����Ϊ�Թ��еĿ�״������̼��ƣ��������Ǹ����Թ��еĿ�����ʵ�����ʱ����ע�������Թ����������������������Ŀ���Ǽ���NO���۲쵽����ɫ���壮