题目内容
【题目】镁及其合金广泛应用于国防生产中。
(1)工业上是通过电解熔融状态![]() 的方法冶炼金属镁的,则
的方法冶炼金属镁的,则![]() 的电子式为___;工业上不用电解熔融MgO来冶炼镁的原因是_____。
的电子式为___;工业上不用电解熔融MgO来冶炼镁的原因是_____。
(2)氢化镁是一种危险化学品。遇湿易燃,其原因是____。
(3)高纯度氧化镁在医药,建筑行业有着广泛的应用,硫酸镁还原热解制备高纯氧化镁是一种新生产工艺,以菱镁矿(主要成分为![]() ,含少量
,含少量![]() )为原料,制备高纯氧化镁的流程如图(已知
)为原料,制备高纯氧化镁的流程如图(已知![]() 、
、![]() ):
):
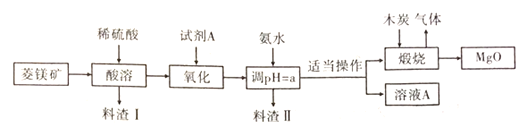
①酸浸前对矿石进行粉碎的好处是____。试剂A是一种绿色氧化剂。常温下为液态,写出“氧化”过程中发生反应的离子方程式_____。
②为除尽杂质,a的取值应不小于___(当杂质离子浓度小于![]() 时,可认为已除尽;
时,可认为已除尽;![]() ≈0.2)。
≈0.2)。
③煅烧过程中可发生多个反应。试写出氧化剂与还原剂按物质的量为2:1的比例恰好反应时的化学方程式_____,反应生成的气体均为____(填“酸性”或“碱性”)氧化物。
【答案】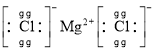 MgO熔点太高,若是以MgO为原料,则生产成本过高
MgO熔点太高,若是以MgO为原料,则生产成本过高 ![]() 与水反应生成易燃的氢气,且反应过程中可能会放出热量使氢气燃烧甚至爆炸 能提高反应速率与浸出率 2Fe2++2H++H2O2=2Fe3++2H2O 3.2 2MgSO4+C
与水反应生成易燃的氢气,且反应过程中可能会放出热量使氢气燃烧甚至爆炸 能提高反应速率与浸出率 2Fe2++2H++H2O2=2Fe3++2H2O 3.2 2MgSO4+C![]() 2MgO+2SO2↑+CO2↑ 酸性
2MgO+2SO2↑+CO2↑ 酸性
【解析】
(1)![]() 为离子化合物,其电子式为
为离子化合物,其电子式为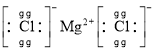 ,MgO熔点太高,若是以MgO为原料,则生产成本过高,故工业不使用MgO作原料冶炼;
,MgO熔点太高,若是以MgO为原料,则生产成本过高,故工业不使用MgO作原料冶炼;
(2)氢化镁是一种危险化学品。遇湿易燃,其原因是MgH2与水反应生成易燃的氢气,且反应过程中可能会放出热量使氢气燃烧甚至爆炸;
(3)①酸浸前对矿石进行粉碎的好处是能提高反应速率与浸出率,“氧化”过程中发生反应为亚铁离子被氧化为三价铁,离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O;
②氢氧化铁固体溶于水存在离子平衡Fe(OH)3(s) ![]() Fe3+(aq)+3OH-(aq),故Fe元素完全沉淀时,
Fe3+(aq)+3OH-(aq),故Fe元素完全沉淀时,![]() ,此时pH为3.2;
,此时pH为3.2;
③煅烧过程中氧化剂为硫酸镁,还原剂为C,方程式为2MgSO4+C![]() 2MgO+2SO2↑+CO2↑,反应生成的气体为酸性氧化物。
2MgO+2SO2↑+CO2↑,反应生成的气体为酸性氧化物。

【题目】对于元素周期表中下列位置的①~⑩十种元素,请回答有关问题(用元素符号或化学式回答)。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | ⑥ | ||||
3 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)在上述元素中,金属性最强的是___,原子半径最大的是___(0族除外)。
(2)用电子式表示⑦和⑩形成的化合物的过程___。
(3)表中元素构成10电子微粒的分子有:___(任写2种)。
(4)⑤和⑨分别与氢原子构成的简单氢化物中沸点最高的是___。
(5)表中元素⑤和⑦可以形成一种淡黄色物质X,写出X的电子式:___,该物质所含化学键类型___,0.1molX与水反应转移电子数为___。
【题目】下列实验操作,现象和结论都正确的是
选项 | 操作 | 现象 | 结论 |
A | 用坩埚钳夹一块铝箔在酒精灯上灼烧 | 铝箔熔化并滴落 | 氧化铝的熔点较低 |
B | 向亚硫酸钠溶液中滴加足量盐酸,将产生的气体通入品红溶液 | 品红溶液褪色 | 非金属性: |
C | 将用砂纸除去保护膜的镁片和铝片(大小、形状相同),分别插入同浓度的稀硫酸中 | 镁片表面产生气泡速率大于铝片 | 还原性: |
D | 常温下,将两根大小相同的铁钉分别插入浓硝酸和稀硝酸中 | 浓硝酸中无明显现象,稀硝酸中产生气泡 | 稀硝酸的氧化性比浓硝酸强 |
A.AB.BC.CD.D