题目内容
1.下列叙述中正确的是( )| A. | 冰融化时水分子中共价键发生断裂 | |
| B. | H2O2、PCl5都是含有极性键的非极性分子 | |
| C. | HF、HCl、HBr、HI的酸性依次增强 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
分析 A.冰融化时克服分子间作用力;
B.H2O2为极性分子;
C.HF、HCl、HBr、HI的共价键依次减弱,易电离;
D.氢键与分子的稳定性无关.
解答 解:A.冰融化为物理变化,克服分子间作用力,故A错误;
B.H2O2结构不对称,正负电荷不重叠,为极性分子,故B错误;
C.HF、HCl、HBr、HI的共价键依次减弱,易电离,溶液酸性增强,故C正确;
D.氢键与分子的稳定性无关,共价键决定分子的稳定性,故D错误.
故选C.
点评 本题综合考查基本概念以及共价键等知识,为高频考点,侧重于双基的考查,注意相关基础知识的学习和积累,难度不大.

练习册系列答案
相关题目
12.将锌片和铜片按图示方式插入柠檬中,当导线中有2mol电子通过,下列针对该装置的说法不正确的是( )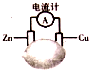

| A. | 锌片溶解了65g | B. | 电子由锌片流出 | ||
| C. | 铜片是负极 | D. | 锌片上发生氧化反应 |
9.已知维生素A 的结构简式可写为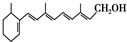 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )| A. | 维生素A的分子式为C20H30O | |
| B. | 维生素A中含有苯环 | |
| C. | 维生素A中可以使溴水褪色 | |
| D. | 1mol维生素A在催化剂作用下最多可与7molH2发生加成反应 |
16.如表是元素周期表的一部分,针对表中的①~⑥元素,回答下列问题
(1)最活泼的金属元素是Na(填元素符号),②和⑤两种元素原子半径较大的是Si(填元素符号),⑤和⑥两种元素最高价氧化物对应的水合物酸性较强的元素是Cl(填元素符号);
(2)写出①单质在⑥单质中燃烧的化学方程式H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl.
(3)①②③三种元素能够形成多种有机化合物,其中一种不仅是厨房调味剂而且还能除去水垢.写出此物质的结构式:CH3COOH;写出该物质与NaHCO3反应的化学方程式:CH3COOH+NaHCO3→CH3COONa+H2O+CO2↑.
 | ⅠA | 0族 | ||||||
| 一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 二 | ② | ③ | ||||||
| 三 | ④ | ⑤ | ⑥ | |||||
(2)写出①单质在⑥单质中燃烧的化学方程式H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl.
(3)①②③三种元素能够形成多种有机化合物,其中一种不仅是厨房调味剂而且还能除去水垢.写出此物质的结构式:CH3COOH;写出该物质与NaHCO3反应的化学方程式:CH3COOH+NaHCO3→CH3COONa+H2O+CO2↑.
6.下列工业生产过程中不涉及氧化还原反应的是( )
①制水泥、玻璃 ②制硝酸 ③制硫酸 ④氯碱工业 ⑤合成氨 ⑥制漂白粉 ⑦制皂.
①制水泥、玻璃 ②制硝酸 ③制硫酸 ④氯碱工业 ⑤合成氨 ⑥制漂白粉 ⑦制皂.
| A. | ①②③⑤ | B. | ①③⑤⑥⑦ | C. | 只有①⑦ | D. | ③⑥⑦ |
13.下列化学反应的离子方程式正确的是( )
| A. | 向FeCl3溶液中加入Cu粉:2Fe3++3Cu═2Fe+3Cu2+ | |
| B. | Cu和稀硝酸反应:Cu+2H++NO3-═Cu2++NO↑+H2O | |
| C. | NaOH溶液中通入少量二氧化硫:SO2+2OH-═SO32-+H2O | |
| D. | 碳酸氢钙溶液和氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2O |
10.下列说法正确的是( )
| A. | 2CH2=CH2+O2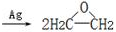 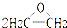 是理想的原子经济,原子利用率为100% 是理想的原子经济,原子利用率为100% | |
| B. | 含磷合成洗涤剂易被细菌分解,故不会导致水体污染 | |
| C. | CO2的大量排放能破坏臭氧层,形成“臭氧空洞” | |
| D. | pH在5.6~7.0之间的降水通常称为酸雨 |