题目内容
12.将锌片和铜片按图示方式插入柠檬中,当导线中有2mol电子通过,下列针对该装置的说法不正确的是( )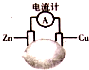
| A. | 锌片溶解了65g | B. | 电子由锌片流出 | ||
| C. | 铜片是负极 | D. | 锌片上发生氧化反应 |
分析 锌比铜活泼,锌为负极,发生氧化反应,电极方程式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极方程式为2H++2e-=H2↑,以此解答.
解答 解:A.负极反应式为Zn-2e-=Zn2+,当导线中有2mol电子通过,消耗1molZn,质量为65g,故A正确;
B.锌为负极,电子由锌片流出,故B正确;
C.较活泼金属为负极,较不活泼金属为正极,铜为正极,故C错误;
D.锌为负极,发生氧化反应,故D正确.
故选C.
点评 本题考查原电池知识,侧重于学生的分析能力和基本概念的考查,为高频考点,有利于培养学生的良好科学素养,提高学习的积极性,难度不大,注意把握原电池的组成条件和工作原理.

练习册系列答案
相关题目
5.下列有关有机物分离提纯或除杂的方法错误的是( )
| A. | 溴苯中混有溴,加NaOH溶液洗涤、静置、分液 | |
| B. | 除去乙醇中少量乙酸:加入足量生石灰蒸馏 | |
| C. | 乙酸乙酯中有乙酸杂质,可以加入饱和Na2CO3溶液,充分反应后静置分液 | |
| D. | 乙烯中混有SO2,将其通过盛有酸性KMnO4溶液的洗气瓶,再干燥 |
6.表示下列反应的离子方程式中,正确的是( )
| A. | 烧碱加入醋酸溶液OH-+CH3COOH═CH3COO-+H2O | |
| B. | 盐酸与小苏打溶液反应2H++CO32-═CO2↑+H2O | |
| C. | 氢氧化钡溶液中加入稀硫酸:Ba2++SO42-═BaSO4↓ | |
| D. | 金属钠与水反应Na+2H2O═Na++2OH-+H2↑ |
7.在某温度时,将n mol•L-1氨水滴入10mL 1.0mol•L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是( )

| A. | a点Kw=1.0×10-14 mol2•L-2 | |
| B. | 水的电离程度:b>c>a>d | |
| C. | b点:C(NH4+)>C(Cl-)>C(H+)>C(OH-) | |
| D. | 25℃时NH4Cl水解常数为(n-1)×10-7 mol•L-1(用n表示) |
17.可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极.下列说法不正确的是( )
| A. | 以NaCl溶液或NaOH溶液为电解液时,正极反应都为O2+2H2O+4e-=4OH- | |
| B. | 以NaOH溶液为电解液时,负极反应为Al+4OH--3e-=AlO2-+2H2O | |
| C. | 以NaOH溶液为电解液时,电池在工作过程中电解液的pH增大 | |
| D. | 以NaCl溶液为电解液时,电流由空气电极沿导线流向铝合金电极 |
4.下列说法正确的是( )
| A. | CaO、H2SO4、NaHCO3、碘酒均属于化合物 | |
| B. | 胶体与溶液的本质区别在于是否产生丁达尔效应 | |
| C. | 合金具有良好的物理、化学和机械性能,熔点比成分金属低 | |
| D. | 计算机芯片、太阳能电池、石英钟表主要材料均为SiO2 |
1.下列叙述中正确的是( )
| A. | 冰融化时水分子中共价键发生断裂 | |
| B. | H2O2、PCl5都是含有极性键的非极性分子 | |
| C. | HF、HCl、HBr、HI的酸性依次增强 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
2.如图所示装置中,电流表G指针发生偏转,同时X极放出气体,Y极逐渐变细.下列判断正确的是( )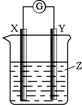

| A. | X是Zn,Y是Cu,Z为稀HCl溶液 | B. | X是Cu,Y是Zn,Z为稀H2SO4溶液 | ||
| C. | X是Cu,Y是石墨,Z为稀AgNO3溶液 | D. | X是石墨,Y是Fe,Z为稀AgNO3溶液 |