题目内容
某同学用下列装置制备并检验Cl2的性质: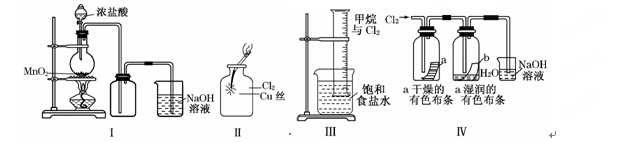
下列说法正确的是( )
| A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗完 |
| B.Ⅱ图中:生成蓝色的烟 |
| C.Ⅲ图中:量筒中发生了加成反应 |
| D.Ⅳ 图中湿润的有色布条能褪色,将浓硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
D
解析试题分析:A、二氧化锰和浓盐酸在加热条件下发生氧化还原反应生成氯气,但稀盐酸与二氧化锰不反应,当盐酸浓度降低时,反应停止,则盐酸不能完全消耗,故A错误;B、氯气与铜反应生成棕黄色的烟,加水溶液呈蓝色,故B错误;C、氯气和甲烷在光照下发生取代反应,故C错误;D、氯气与水反应生成具有漂白性的HClO,湿润的有色布条能褪色,与NaOH反应生成NaCl和NaClO,二者在酸性条件下反应生成氯气,故D正确,故选D。
考点:考查氯气的性质实验探究

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
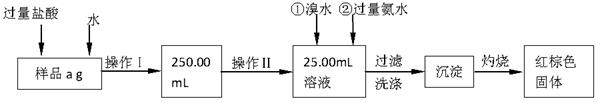
铁触媒(铁的氧化物)是硫酸工业的催化剂。某同学设计了以下两种方案研究铁触媒的组成。
方案一:用下列装置测定铁触媒的含铁量,确定其组成。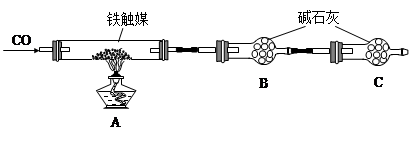
方案二:用下列实验方法测定铁触媒的含铁量,确定其组成。
(1)步骤④中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和 。
(2)因为通入Cl2不足量,“溶液B”中还含有 会影响测定结果。
(3)因为通入Cl2过量且加热煮沸不充分,“溶液B”中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。
限选试剂:0.1mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红稀溶液、淀粉-KI溶液、0.1moL·L-1KSCN溶液
| 实验操作 | 实验现象与结论 |
| | |
(4)“干燥管C”的作用是 。
(5)称取15.2g铁触媒进行上述实验。充分反应后,测得“干燥管B”增重11.0g,则该铁触媒的化学式可表示为 。
碘在地壳中主要以NaIO3的形式存在,在海水中主要以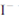 的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法不正确的是
的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法不正确的是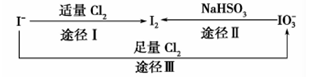
| A.可用KI淀粉试纸和食醋检验加碘盐中是否含有碘 |
B.足量Cl2能使湿润的KI淀粉试纸变白的原因可能是 |
C.由图可知氧化性的强弱顺序为 |
D.途径Ⅱ中若生成1molI2,反应中转移的电子数为10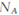 |
下列试剂中,不能贮存在玻璃瓶中的是
| A.浓硫酸 | B.氢氟酸 | C.浓氢氧化钠溶液 | D.硝酸银溶液 |
下列溶液中:①石灰水 ②Na2S溶液 ③KMnO4溶液 ④溴水 ⑤酸化的Ba(NO3)2溶液
⑥品红溶液,不能区别SO2和CO2气体的是( )
| A.只有① | B.①② | C.①②⑤ | D.②④⑤ |
下列有关物质性质的应用正确的是
| A.石英坩埚耐高温,可用来加热熔化NaOH固体 |
| B.浓硫酸有脱水性,可用作干燥剂 |
| C.二氧化硫有漂白性,可大量用于加工食品使食品漂白 |
| D.医用酒精能使蛋白质变性,可用来消毒杀菌 |