题目内容
下列有关物质性质的应用正确的是
| A.石英坩埚耐高温,可用来加热熔化NaOH固体 |
| B.浓硫酸有脱水性,可用作干燥剂 |
| C.二氧化硫有漂白性,可大量用于加工食品使食品漂白 |
| D.医用酒精能使蛋白质变性,可用来消毒杀菌 |
D
解析试题分析:A、石英坩埚中的SiO2是酸性氧化物,与NaOH反应,所以不能用石英坩埚加热融化NaOH固体,错误;B、浓硫酸作干燥剂是利用了浓硫酸具有吸水性的性质,错误;C、二氧化硫有毒,不能用于加工食品使食品漂白,错误;D、医用酒精能使蛋白质变性,可用来消毒杀菌,正确。
考点:本题考查物质的性质与用途。

练习册系列答案
相关题目
某同学用下列装置制备并检验Cl2的性质: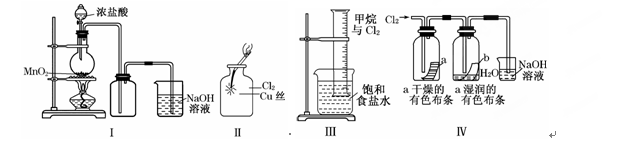
下列说法正确的是( )
| A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗完 |
| B.Ⅱ图中:生成蓝色的烟 |
| C.Ⅲ图中:量筒中发生了加成反应 |
| D.Ⅳ 图中湿润的有色布条能褪色,将浓硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
下列说法或做法错误的是
| A.充满NH3的烧瓶倒置于水中后液面迅速上升,说明NH3易溶于水 |
| B.在胆矾中滴加浓H2SO4,固体变白,说明浓H2SO4具有吸水性 |
| C.将二氧化硫通入品红溶液,溶液褪色,加热后能恢复原色 |
| D.向铜粉中加入浓硫酸,加热,铜粉溶解,同时产生H2 |
向淀粉溶液中分别加入下列物质,能使溶液变蓝的是
| A.氯水 | B.溴水 | C.碘化钾 | D.碘水 |
下列化学实验事实及其结论都正确的是
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化性 |
| D | 将SO2通入溴水中,酸性高锰酸钾溶液褪色 | SO2具有漂白性 |
海带中的碘元素是以I-的形式存在的,为将I-转化成I2并提取出来,设计操作步骤如下:①通入Cl2;②将海带烧成灰,向灰中加水,搅拌;③加CCl4振荡;④过滤;⑤用分液漏斗分液。合理的操作顺序为( )
| A.①③⑤②④ | B.②①③④⑤ | C.②④①③⑤ | D.③①②⑤④ |
在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
| A.氯水的颜色呈浅绿色,说明氯水中含有Cl2 |
| B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- |
| C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
| D.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO |
下列说法中正确的是 ( )
| A.6.8 g固体KHSO4与3.9 g固体Na2O2中阴离子数目相同 |
| B.常温下铁、铜均不溶于浓硫酸, 说明常温下铁、铜与浓硫酸均不反应 |
| C.离子化合物中只含离子键 |
| D.中子数为18的氯原子可表示为18Cl |
为证明稀硝酸与铜反应产物中气体为NO,设计如图实验(实验过程中活塞2为打开状态),下列说法中不正确的是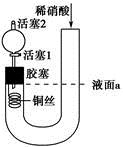
| A.关闭活塞1,加入稀硝酸至液面a处 |
| B.在装置左侧稍加热可以加快稀硝酸与铜的反应速率 |
| C.通过关闭或开启活塞1可以控制反应的进行 |
| D.反应开始后,胶塞下方有无色气体生成,还不能证明该气体为NO |