题目内容
【题目】当今环境问题越来越受到人们的重视。汽车尾气中含有较多的NO和CO,两种气体均会使人体中毒。处理大气中的污染物,打响“蓝天白云”保卫战是当前的重要课题。请回答下列问题
(1)用还原法将NO转化为无污染的物质。已知:
2C(s)+O2(g)![]() 2CO △H1=-221.0KJ/mol
2CO △H1=-221.0KJ/mol
N2(g)+O2(g)![]() 2NO △H2=+180.5KJ/mol
2NO △H2=+180.5KJ/mol
2NO+C(s)![]() CO2(g)+N2(g) △H3=-573.75KJ/mol
CO2(g)+N2(g) △H3=-573.75KJ/mol
请写出CO与NO生成无污染气体CO2与N2的热化学方程式_______________________。
(2)在一定温度下,向甲、乙、丙三个恒容密闭容器中加入一定量的NO和足量的焦炭,反应过程中测得各容器中c(NO)(mol/L)随时间(s)的变化如下表。
已知:三个容器的反应温度分别为T甲= 500℃、T乙= 500℃、T丙= a℃
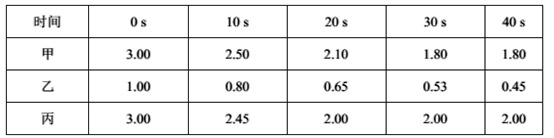
甲容器中,该反应的平衡常数K=_______。丙容器的反应温度a _______500℃(填“”、“<”或“=”),理由是_______________________________。
(3)某研究性小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。
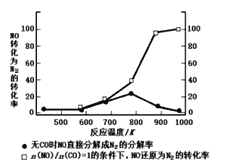
①若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因为_________。
②在n(NO)/n(CO)=1的条件下,为更好的除去NO物质,应控制的最佳温度在_____K左右。
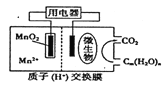
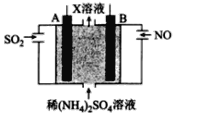
(4)利用电解原理也可以处理NO。下图为工业生产模拟装置。其中A、B为多孔电极(外接电源未画出),则B为___________极(填“正”“负”“阴”或“阳”,),A电极反应式为______________________。
【答案】2CO(g)+2NO(g) ![]() 2CO2(g)+ N2(g)△H=-746.0 kJ/mol
2CO2(g)+ N2(g)△H=-746.0 kJ/mol ![]() > 甲、丙容器中反应物起始量相同,丙容器达平衡的时间比甲容器达平衡的时间短 NO的分解反应是放热反应,升高温度不利于正反应进行 870K(温度写到800K~900K之间均可) 阴极 SO2-2e+2H2O= SO42 +4H+
> 甲、丙容器中反应物起始量相同,丙容器达平衡的时间比甲容器达平衡的时间短 NO的分解反应是放热反应,升高温度不利于正反应进行 870K(温度写到800K~900K之间均可) 阴极 SO2-2e+2H2O= SO42 +4H+
【解析】
(1)根据盖斯定律进行分析;
(2)根据三段式,计算出平衡时各物质的浓度,根据平衡常数计算公式K= ![]() 进行计算;根据温度对反应速率的影响规律进行分析;
进行计算;根据温度对反应速率的影响规律进行分析;
(3)①根据温度对平衡移动的规律进行分析;
②在![]() =1的条件下,根据图像可知,温度在870K左右分解率几乎达到100%;
=1的条件下,根据图像可知,温度在870K左右分解率几乎达到100%;
(4)根据图示,A极SO2失电子发生氧化反应生成SO42,则A为阳极,发生氧化反应。
(1)已知:①2C(s)+O2(g)![]() 2CO △H1=-221.0kJ/mol
2CO △H1=-221.0kJ/mol
②N2(g)+O2(g)![]() 2NO △H2=+180.5kJ/mol
2NO △H2=+180.5kJ/mol
③2NO+C(s)![]() CO2(g)+N2(g) △H3=-573.75kJ/mol
CO2(g)+N2(g) △H3=-573.75kJ/mol
CO与NO生成气体CO2与N2的热化学方程式为2CO(g)+2NO(g) ![]() 2CO2(g)+ N2(g)△H,根据盖斯定律可知2③-(①-②)可得目标反应方程式,所以△H=-573.75kJ/mol×2-(-221.0kJ/mol-180.5kJ/mol)=-746.0 kJ/mol,所以该反应的热化学方程式为:2CO(g)+2NO(g)
2CO2(g)+ N2(g)△H,根据盖斯定律可知2③-(①-②)可得目标反应方程式,所以△H=-573.75kJ/mol×2-(-221.0kJ/mol-180.5kJ/mol)=-746.0 kJ/mol,所以该反应的热化学方程式为:2CO(g)+2NO(g) ![]() 2CO2(g)+ N2(g)△H=-746.0 kJ/mol;
2CO2(g)+ N2(g)△H=-746.0 kJ/mol;
(2)甲容器中,发生反应2NO(g)+C(s) ![]() CO2(g)+ N2(g),根据容器中cNO) (mol/L)随时间(s)的变化,列三段式:
CO2(g)+ N2(g),根据容器中cNO) (mol/L)随时间(s)的变化,列三段式:
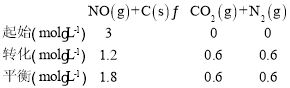
根据平衡常数的定义可知K=![]() =
=![]() ;
;
甲、丙容器中反应物起始量相同,丙容器达平衡的时间比甲容器达平衡的时间短,反应速率更快,故丙容器的反应温度a > 500℃;
(3)①根据图像可知,温度超过775K,升高温度, NO的分解率降低,平衡逆向移动,则NO的分解反应为放热反应;
②在![]() =1的条件下,根据图像可知,温度在870K左右分解率几乎达到100%,且再继续升高温度,分解率变化不大;
=1的条件下,根据图像可知,温度在870K左右分解率几乎达到100%,且再继续升高温度,分解率变化不大;
(4)根据图示,A极SO2失电子发生氧化反应生成SO42-,则A为阳极,电极反应式是SO2-2e+2H2O=SO42-+4H+,则B为阴极。