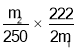题目内容
【题目】锰不仅在工业上用途广泛,还是人体内必需的微量元素,对人体健康起着重要的作用。一种以天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)为原料制备金属锰的流程如图所示。请回答下列问题:
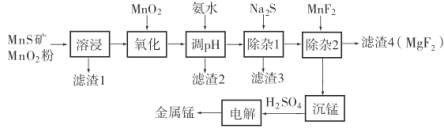
相关金属离子![]() 形成氢氧化物沉淀的pH范围如下:
形成氢氧化物沉淀的pH范围如下:
金属离子 |
|
|
|
|
|
|
|
开始沉淀pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“溶浸”中需加入的试剂是________(填化学式)。
(2)“调pH”除铁和铝,溶液的pH范围应调节为________~6之间。
(3)“滤渣2”的主要成分是________________________________(填化学式)。
(4)![]() 可做“沉锰”试剂,该物质的水溶液呈碱性,其溶液中离子浓度由大到小的顺序为________________________________。
可做“沉锰”试剂,该物质的水溶液呈碱性,其溶液中离子浓度由大到小的顺序为________________________________。
(5)“沉锰”得到![]() 沉淀,写出该反应的离子方程式________________。
沉淀,写出该反应的离子方程式________________。
(6)电解硫酸锰溶液制备单质锰时,阴极的电极反应为________;电解后的电解质溶液可返回________工序继续使用。
【答案】![]() 4.7
4.7 ![]() 、
、![]()
![]()
![]()
![]() 溶浸
溶浸
【解析】
天然二氧化锰粉与硫化锰矿与硫酸反应,过滤出不溶于硫酸的物质,再加二氧化锰氧化亚铁离子,再加氨水调节溶液的pH除掉铝离子和铁离子,再加硫化钠除掉镍离子和锌离子,过滤,向滤液中加入氟化锰除掉镁离子,过滤,再加碳酸氢铵沉锰,得到碳酸锰,碳酸锰加硫酸反应生成硫酸锰,再电解得到锰和硫酸,硫酸反复使用。
(1)根据后面沉锰时加硫酸,因此再“溶浸”中需加入的试剂是硫酸;故答案为:H2SO4。
(2)“调pH”除铁和铝,将铝离子生成沉淀,完全沉淀pH为4.7,因此溶液的pH范围应调节为4.7~6之间;故答案为:4.7。
(3) 调节为4.7~6之间,因此“滤渣2”的主要成分是![]() 、
、![]() ;故答案为:
;故答案为:![]() 、
、![]() 。
。
(4)![]() 可做“沉锰”试剂,该物质的水溶液呈碱性,说明碳酸氢根水解程度大于铵根水解程度,因此溶液中离子浓度由大到小的顺序为
可做“沉锰”试剂,该物质的水溶液呈碱性,说明碳酸氢根水解程度大于铵根水解程度,因此溶液中离子浓度由大到小的顺序为![]() ;故答案为:
;故答案为:![]() 。
。
(5)“沉锰”是锰离子和碳酸氢根反应生成![]() 沉淀、二氧化碳和水,其反应的离子方程式
沉淀、二氧化碳和水,其反应的离子方程式![]() ;故答案为:
;故答案为:![]() 。
。
(6)电解硫酸锰溶液制备单质锰时,阴极是锰离子得到电子,其电极反应为![]() ;阳极得到硫酸,因此电解后的电解质溶液可返回溶浸工序继续使用;故答案为:
;阳极得到硫酸,因此电解后的电解质溶液可返回溶浸工序继续使用;故答案为:![]() ;溶浸。
;溶浸。

【题目】将炼钛厂、氯碱厂和甲醇厂组成产业链如下,可得到烧碱、甲醇、钛以及其他一些有用的副产品。
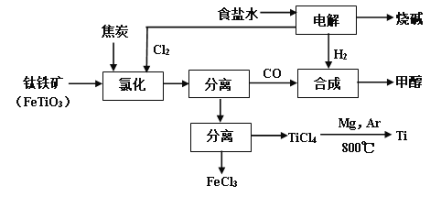
已知:合成甲醇的主反应为:CO+2H2![]() CH3OH+Q(Q>0,下同);
CH3OH+Q(Q>0,下同);
同时有副反应如:8CO+17H2![]() C8H18+8H2O+Q;4CO+8H2
C8H18+8H2O+Q;4CO+8H2![]() C4H9OH+3H2O+Q。
C4H9OH+3H2O+Q。
请完成下列填空:
(1)在实验室电解饱和食盐水时,因工业食盐中含有少量氯化钙、硫酸镁等杂质,除杂时先加入沉淀剂,然后过滤,滤渣的成分是__________(填写化学式)。
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式_________。
(3)诸如上述联合生产,其优点有_______。生产中除了获得上述目标产品外,还能得到副产品________(填写化学式)。
(4)在上述产业链中,合成192吨甲醇理论上需额外补充H2 _____吨(不考虑生产过程中物质的损失及副反应)。
(5)上述产业链中“氯化”在6000C以上的反应器内进行。已知:
物质 | 沸点(0C) |
TiCl4 | 136 |
FeCl3 | 315 |
为了将TiCl4从“氯化”后的混合物中分离出来,请设计合理的方案:_______。
【题目】高炉炼铁过程中发生反应:![]() ,该反应在不同温度下的平衡常数见表。下列说法正确的是( )
,该反应在不同温度下的平衡常数见表。下列说法正确的是( )
温度T/℃ | 1000 | 1150 | 1300 |
平衡常数K | 4.0 | 3.7 | 3.5 |
A.平衡后温度不变缩小容器容积,![]() 的转化率升高
的转化率升高
B.增加高炉的高度可以有效降低炼铁尾气中CO的含量
C.其他条件不变时,增大c(CO),该反应的K值增大
D.由表中数据可判断该反应:反应物总能量大于生成物的总能量
【题目】“中和滴定”原理在实际生产生活中应用广泛。用![]() 可定量测定CO的含量,该反应原理为
可定量测定CO的含量,该反应原理为![]() ,其实验步骤如下:
,其实验步骤如下:
①取200 mL(标准状况)含有CO的某气体样品通过盛有足量![]() 的硬质玻璃管中在170℃下充分反应:
的硬质玻璃管中在170℃下充分反应:
②用酒精溶液充分溶解产物![]() ,配制100 mL溶液;
,配制100 mL溶液;
③量取步骤②中溶液20.00 mL于锥形瓶中,然后用![]() 的
的![]() 标准溶液滴定,发生反应为
标准溶液滴定,发生反应为![]() 。消耗标准
。消耗标准![]() 溶液的体积如表所示。
溶液的体积如表所示。
第一次 | 第二次 | 第三次 | |
滴定前读数/mL | 1.10 | 1.50 | 2.40 |
滴定后读数/mL | 21.00 | 21.50 | 22.50 |
(1)步骤②中配制100 mL待测液需要用到的玻璃仪器的名称是烧杯、量筒、玻璃棒、胶头滴管和________。
(2)![]() 标准液应装在________(填“酸式”“碱式”)滴定管中。
标准液应装在________(填“酸式”“碱式”)滴定管中。
(3)指示剂应选用________,判断达到滴定终点的现象是________。
(4)气体样品中CO的体积分数为________(已知气体样品中其他成分不与![]() 反应)
反应)
(5)下列操作会造成所测CO的体积分数偏大的是________(填字母)。
a.滴定终点时仰视读数
b.滴定前尖嘴外无气泡,滴定后有气泡
C.配制100 mL待测溶液时,有少量溅出。
d.锥形瓶用待测溶液润洗