题目内容
工业上用白云石制备高纯氧化镁的工艺流程如下:
已知白云石的主要成分可表示为:
CaO 32.50%;MgO 20.58%;Fe2O3 2.18%;SiO2 0.96%;其他 43.78%
(1)为了提高白云石的煅烧效果,可以采取的措施是 。
若在实验室中煅烧白云石,需要的仪器除酒精灯、三脚架以外,还需要 。
| A.蒸发皿 | B.坩埚 | C.泥三角 | D.石棉网 |

(3)从溶液中获得CaSO4·2H2O的操作是蒸发浓缩、 、过滤、洗涤、干燥。
(4)写出沉淀反应中的离子方程式: 。检验沉淀是否洗净的方法是: 。
(5)沉淀反应过程中,温度对产品的纯度也有一定的影响。如图为反应温度对氧化镁纯度的影响。最终确定本反应的适宜温度为 。

(1)矿石粉碎(2分)BC(2分,选对1个给1分,错选不得分)
(2)Mg(OH)2或MgO未完全溶解(2分);产品纯度下降(合理答案均给分)(2分)
(3)冷却结晶(或结晶)(1分)
(4)Mg2++2NH3·H2O=Mg(OH)2↓+2NH4+(2分)
取最后一次洗涤液,加BaCl2溶液,无沉淀则洗净(2分)
(5)40℃(2分)
解析试题分析:(1)矿石粉碎,增大接触面积,充分反应;加热固体需用坩埚及三脚架、泥三角等;(2)pH过高会Mg(OH)2或MgO未完全溶解,从而是镁浸取率降低;pH过低会导致氧化铁等杂质溶解形成杂质导致产品纯度降低;(3)降温结晶或冷却结晶,不能用蒸发结晶;(4)氨水与镁离子的反应,取最后一次洗涤液,加BaCl2溶液,无沉淀则洗净;(5)取纯度最高时的温度。
考点:考查工业流程中实验条件的选择、操作的仪器及操作方法等有关问题。

我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):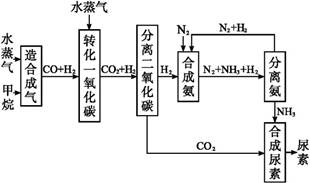
请填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在t℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量。该反应的热化学方程式是 。
(2)上述流程中,工业上分离H2、CO2合理的方法是 。
| A.混合气先通入氢氧化钠溶液,再在溶液中加入盐酸 |
| B.混合气加压冷却,使CO2液化 |
| C.混合气用氨水洗涤 |
| D.混合气先通入石灰浆中,然后高温煅烧固体 |
(4)合理地利用资源不仅可以提高经济效益,也是对社会、对全人类负责的表现,请用线段和箭头画出图中的两处合理利用资源情况。
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g) 2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是 ( )。
2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是 ( )。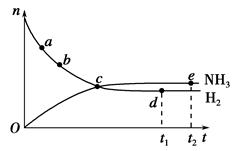
| A.点a的正反应速率比点b的小 |
| B.点c处反应达到平衡 |
| C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D.其他条件不变,773 K下反应至t1时刻,n(H2)比上图中d点的值大 |

 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。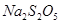 )常用作食品漂白剂,其制备工艺流程如下:
)常用作食品漂白剂,其制备工艺流程如下: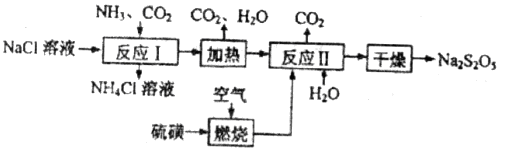
 等多步反应。
等多步反应。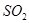 ,其离子方程式为___________。
,其离子方程式为___________。
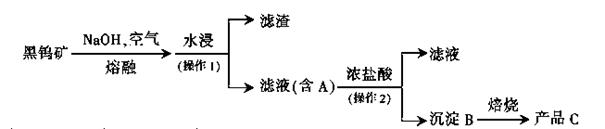


 Li7Ti5O12+3FePO4
Li7Ti5O12+3FePO4