题目内容
将0.1mol·L-1K2SO4溶液、0.2mol·L-1Fe2(SO4)3溶液与水混合,欲使混合溶液中K+、Fe3+、SO42-物质的量浓度为0.1mol·L-1、0.1mol·L-1、0.2mol·L-1,则所用的K2SO4溶液,Fe2(SO4)3溶液、水的体积比约为( )
| A.1:1:1 | B.2:1:1 | C.1:1:2 | D.2:1:2 |
B
解析试题分析:1L的0.1mol·L-1的K2SO4溶液K+有0.2mol, SO42-0.2mol,1L的0.2mol·L-1的Al2(SO4)3溶液, Al3+0.4mol。但K+、Al3+浓度分别为0.1mol·L-1、0.1mol·L-1。所以其K+、Al3+体积比2比1才可,K+2L,Al3+1L此时两者都是0.4mol, SO42-为0.8mol,所以加水1L,才使K+、Al3+、SO42-的浓度为0.1mol·L-1、0.1mol·L-1、0.2mol·L-1。故选B。
考点:化学计算

下列有关化学用语使用正确的是( )
A.CO2的电子式: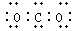 |
| B.次氯酸的结构式: H—O—Cl |
C.中子数为18的氯原子结构示意图: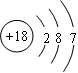 |
| D.二氧化硅的分子式为:SiO2 |
实验室需要2.0 mol·L-1NaOH溶液90mL,请回答下列问题:
(1)配制过程中不需要使用到的化学仪器有 (填字母)
| A.烧杯 | B.100mL容量瓶 | C.漏斗 | D.胶头滴管 E.玻璃棒 |
(3)下列主要操作步骤的正确顺序是 (填序号);
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1—2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到100mL容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量的蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中;
(4)在实验中其他操作均正确,如实验过程中缺少步骤⑤,会使配制出的NaOH溶液浓度 (填“偏高”或“偏低”或“不变”);若定容时仰视刻度线,则所得溶液浓度 2.0 mol·L-1(填“大于”或“小于”或“等于”)。
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2L的水中含有0.5个NA水分子 |
| B.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Mg2+的个数为0.5NA |
| C.1 mol H2和O2的混合气体中含NA个分子 |
| D.11.2L NH3中所含的原子数目为2NA |
铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混和、压制,就可以制成铅笔芯。如果铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为0.5mg。那么一个铅笔字含有的碳原子数约为( )
| A.2.5×1019个 | B.2.5×1022个 | C.1.25×1019个 | D.1.25×1022个 |
下列说法正确的是(NA表示阿伏加德罗常数的值) ( )
| A.1.8g NH4+所含质子数为NA |
| B.通常状况下,NA个CO2分子占有的体积为22.4 L |
| C.物质的量浓度为0.5mol/L的BaCl2溶液中,含有Cl-个数为NA |
| D.1 mol·L-1的CaCl2溶液中,Cl-的物质的量浓度为2 mol·L-1 |
如图所示装置,室温下密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于( )
①2∶7 ②5∶4 ③4∶5 ④7∶2
| A.①② | B.③④ | C.②④ | D.①③ |
下列各项值最精确的是( )
| A.S.T.P下,1mol任何气体的体积为22.4L |
| B.阿佛加德常数为6.02×1023/mol |
| C.设NA代表阿佛加德罗常数,则1mol H2分子数为NA个 |
| D.S.T.P下,0.5mol CO2的体积为11.2L。 |
将8g铁片放入100 mL CuSO4溶液中,Cu2+全部被置换后,取出附有铜的铁片洗涤、干燥、称重,其质量变为8.2g,则原溶液中CuSO4的物质的量浓度是
| A.0.125ol/L | B.0.175mol/L | C.0.25 mol/L | D.0.5 mol/L |