题目内容
某强酸性溶液X中还可能含有Fe2+、Al3+、NH4+、AlO2-、CO32-、SO42-,SiO32-、Cl-、H2SO3中的若干种,现取X溶液进行连续实验,实验过程及产物如下:

下列说法上正确的是( )

下列说法上正确的是( )
| A、由实验①可知,气体A一定是NO,沉淀C一定是BaSO4,原溶液中肯定含有Fe2+ |
| B、由实验②可知,气体D一定是NH3,原溶液中肯定含有NH4+,肯定不含Al3+ |
| C、由实验③可知,沉淀G可能是Al(OH)3和BaCO3 |
| D、原溶液中肯定含有Al3+,NH4+、H2SO3不能确定是否含有SO42- |
考点:常见离子的检验方法
专题:离子反应专题
分析:强酸性溶液中一定不存在与氢离子反应的离子:AlO2-、CO32-、SiO32-,一定存在H2SO3;
X的溶液中加入过量硝酸钡溶液,生成气体A、溶液B和沉淀C,气体A一定NO,原溶液中一定存在Fe2+,沉淀C为硫酸钡;
溶液B中加入过量氢氧化钠生成气体D,D为氨气,则原溶液中一定含有NH4+;
F溶液中通入过量二氧化碳产生沉淀G和溶液F,沉淀G一定为氢氧化铝,原溶液中一定含有Al3+,
根据以上分析进行解答.
X的溶液中加入过量硝酸钡溶液,生成气体A、溶液B和沉淀C,气体A一定NO,原溶液中一定存在Fe2+,沉淀C为硫酸钡;
溶液B中加入过量氢氧化钠生成气体D,D为氨气,则原溶液中一定含有NH4+;
F溶液中通入过量二氧化碳产生沉淀G和溶液F,沉淀G一定为氢氧化铝,原溶液中一定含有Al3+,
根据以上分析进行解答.
解答:
解:强酸性溶液中一定不存在:AlO2-、CO32-、SiO32-,一定存在H2SO3;
将X的溶液中加入过量硝酸钡溶液,生成气体A、溶液B和沉淀C,由于不存在碳酸根离子,则气体A只能为NO,发生了氧化还原反应,原溶液中一定存在具有还原性的Fe2+,沉淀C为硫酸钡;
溶液B中加入过量氢氧化钠生成气体D,则气体D为氨气,原溶液中一定含有NH4+;
F溶液中含有钡离子和氢氧根离子,通入过量的二氧化碳产生沉淀G和溶液F,沉淀G只能为氢氧化铝,原溶液一定含有Al3+,
A.根据以上分析可知,气体A一定是NO,沉淀C一定是BaSO4,原溶液中肯定含有Fe2+,故A正确;
B.由实验②可知,气体D一定是NH3,原溶液中肯定含有NH4+,根据③可知,一定存在铝离子,故B错误;
C.由于二氧化碳过量,则沉淀G一定不会碳酸钡,沉淀G为氢氧化铝,故C错误;
D.根据分析可知,原溶液中一定存在Al3+,NH4+、H2SO3,不能确定是否含有硫酸根离子,故D正确;
故选AD.
将X的溶液中加入过量硝酸钡溶液,生成气体A、溶液B和沉淀C,由于不存在碳酸根离子,则气体A只能为NO,发生了氧化还原反应,原溶液中一定存在具有还原性的Fe2+,沉淀C为硫酸钡;
溶液B中加入过量氢氧化钠生成气体D,则气体D为氨气,原溶液中一定含有NH4+;
F溶液中含有钡离子和氢氧根离子,通入过量的二氧化碳产生沉淀G和溶液F,沉淀G只能为氢氧化铝,原溶液一定含有Al3+,
A.根据以上分析可知,气体A一定是NO,沉淀C一定是BaSO4,原溶液中肯定含有Fe2+,故A正确;
B.由实验②可知,气体D一定是NH3,原溶液中肯定含有NH4+,根据③可知,一定存在铝离子,故B错误;
C.由于二氧化碳过量,则沉淀G一定不会碳酸钡,沉淀G为氢氧化铝,故C错误;
D.根据分析可知,原溶液中一定存在Al3+,NH4+、H2SO3,不能确定是否含有硫酸根离子,故D正确;
故选AD.
点评:本题看出来了常见离子共存、常见离子的检验,题目难度中等,注意掌握常见离子的性质及检验方法,明确离子共存的条件,正确分析反应流程为解答本题的关键.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
下列分子中,所有原子的最外层均为8电子结构的是( )
| A、BeCl2 |
| B、H2S |
| C、光气(COCl2) |
| D、PCl5 |
下列说法正确的是( )
| A、HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 | ||||
| B、原子最外层电子数为2的元素一定处于元素周期表ⅡA族 | ||||
| C、NaOH和Na2O中所含的化学键类型完全相同 | ||||
D、
|
下列各组物质,其中属于同系物的是( )
(1)乙烯和苯乙烯 (2)丙烯酸和油酸 (3)乙醇和丙二醇 (4)丁二烯与异戊二烯
(5)蔗糖与麦芽糖.
(1)乙烯和苯乙烯 (2)丙烯酸和油酸 (3)乙醇和丙二醇 (4)丁二烯与异戊二烯
(5)蔗糖与麦芽糖.
| A、(1)(2)(3)(4) |
| B、(2)(4) |
| C、(1)(2)(4)(5) |
| D、(1)(2)(4) |
将2mol A和2mol B通入一密闭容器中,在某温度下达到平衡:2A(g)+B(g)?2C(g)+D(g).经测定,平衡时混合气体中C的体积分数为24%,则B的转化率为( )
| A、73% | B、24% |
| C、36% | D、12% |
下列实验能成功的是( )
| A、将浓硫酸和乙醇混合加热140℃制乙烯 |
| B、用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热,产生砖红色沉淀 |
| C、CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 |
| D、苯和浓溴水反应制溴苯 |
将2molX和2molY充入2L密闭容器中发生如下反应:X(气)+3Y(气)?2Z(气)+aQ(气),2min达到平衡时生成0.8molZ,测得Q的浓度为0.4mol/L,下列叙述错误是( )
| A、平衡时X的浓度为0.2mol?L-1 |
| B、a的值为2 |
| C、反应速率v(Y)=0.3mol?(L?min)-1 |
| D、Y的转化率为60% |
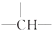 和一个-Cl,它的可能结构分别是
和一个-Cl,它的可能结构分别是