题目内容
用学过的方程式解释下列问题.
(1)用离子方程式解释实验室盛装碱性溶液的试剂瓶用橡皮塞而不用玻璃塞的原因: .
(2)用化学方程式解释漂白粉保存时应干燥的原因: .
(3)硫、氮的氧化物是主要的大气污物,对大气的影响之一是导致酸雨.用化学方程式表示SO2形成酸雨的原因 .
(1)用离子方程式解释实验室盛装碱性溶液的试剂瓶用橡皮塞而不用玻璃塞的原因:
(2)用化学方程式解释漂白粉保存时应干燥的原因:
(3)硫、氮的氧化物是主要的大气污物,对大气的影响之一是导致酸雨.用化学方程式表示SO2形成酸雨的原因
考点:化学方程式的书写,氯、溴、碘及其化合物的综合应用,臭氧,硅和二氧化硅
专题:化学用语专题
分析:(1)玻璃中的二氧化硅与碱反应生成硅酸钠,具有粘合性;
(2)工业用石灰乳和氯气反应制备漂白粉,漂白粉中含有Ca(ClO)2,易与空气中的水和二氧化碳反应生成不稳定的HClO而变质;
(3)SO2气体在空气中经粉尘催化氧化为SO3,SO3与水生成硫酸;或二氧化硫与水反应生成亚硫酸,又被氧化为硫酸;
(2)工业用石灰乳和氯气反应制备漂白粉,漂白粉中含有Ca(ClO)2,易与空气中的水和二氧化碳反应生成不稳定的HClO而变质;
(3)SO2气体在空气中经粉尘催化氧化为SO3,SO3与水生成硫酸;或二氧化硫与水反应生成亚硫酸,又被氧化为硫酸;
解答:
解:(1)玻璃中的二氧化硅与碱反应SiO2+2NaOH═Na2SiO3+H2O,生成硅酸钠具有粘合性,所以不用玻璃塞,离子反应为SiO2+2OH-=SiO32-+H2O,
故答案为:SiO2+2OH-=SiO32-+H2O;
(2)漂白粉中含有Ca(ClO)2,易与空气中的水和二氧化碳反应生成不稳定的HClO,次氯酸见光易分解,反应的相关方程式为Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO、2HClO
2HCl+O2↑,
故答案为:Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO、2HClO
2HCl+O2↑;
(3)SO2气体在空气中经粉尘催化氧化为SO3,SO3与水反应能生成硫酸,有关反应的化学方程式为:2SO2+O2
2SO3;SO3+H2O═H2SO4,或二氧化硫与水反应生成亚硫酸,又被氧化为硫酸,则SO2形成硫酸型酸雨的反应为SO2+H2O?H2SO3、2H2SO3+O2═2H2SO4,
故答案为:2SO2+O2
2SO3;SO3+H2O═H2SO4;或SO2+H2O?H2SO3、2H2SO3+O2═2H2SO4;
故答案为:SiO2+2OH-=SiO32-+H2O;
(2)漂白粉中含有Ca(ClO)2,易与空气中的水和二氧化碳反应生成不稳定的HClO,次氯酸见光易分解,反应的相关方程式为Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO、2HClO
| ||
故答案为:Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO、2HClO
| ||
(3)SO2气体在空气中经粉尘催化氧化为SO3,SO3与水反应能生成硫酸,有关反应的化学方程式为:2SO2+O2
| ||
故答案为:2SO2+O2
| ||
点评:本题考查离子反应及化学反应方程式,明确发生的化学反应是解答本题的关键,注意离子反应的书写方法,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
对于可逆反应A(g)+3B(g)?2C(g),在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
| A、v(A)=0.5mol?L-1?min-1 |
| B、v(B)=1.2mol?L-1?min-1 |
| C、v(C)=0.4mol?L-1?min-1 |
| D、v(C)=1.1mol?L-1?min-1 |
下列各组分子中,均含有非极性键且属于非极性分子的是( )
| A、Cl2 C2H4 |
| B、C2H4 CH4 |
| C、CO2 H2S |
| D、NH3 HCl |
下列化学用语及其说法正确的是( )
| A、H、D、T互为同素异形体,化学性质几乎完全相同 |
B、硫离子结构示意图: |
| C、吸氧腐蚀的正极反应式为:O2+2H2O+4e-═4OH- |
D、NaOH的电子式为: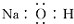 |
试判断C5H12O的同分异构体的种数( )
| A、8 | B、10 | C、13 | D、14 |
某强酸性溶液X中还可能含有Fe2+、Al3+、NH4+、AlO2-、CO32-、SO42-,SiO32-、Cl-、H2SO3中的若干种,现取X溶液进行连续实验,实验过程及产物如下:

下列说法上正确的是( )

下列说法上正确的是( )
| A、由实验①可知,气体A一定是NO,沉淀C一定是BaSO4,原溶液中肯定含有Fe2+ |
| B、由实验②可知,气体D一定是NH3,原溶液中肯定含有NH4+,肯定不含Al3+ |
| C、由实验③可知,沉淀G可能是Al(OH)3和BaCO3 |
| D、原溶液中肯定含有Al3+,NH4+、H2SO3不能确定是否含有SO42- |
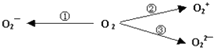 据2004年1月17日网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子
据2004年1月17日网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子