题目内容
下列说法正确的是( )
| A、HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 | ||||
| B、原子最外层电子数为2的元素一定处于元素周期表ⅡA族 | ||||
| C、NaOH和Na2O中所含的化学键类型完全相同 | ||||
D、
|
考点:非金属在元素周期表中的位置及其性质递变的规律,化学键
专题:元素周期律与元素周期表专题
分析:A.元素的非金属性越强,对应的氢化物越稳定,还原性越弱;
B.原子最外层电子数为2的元素可能为He、ⅡA族、ⅡB族等元素;
C.NaOH含有离子键和共价键;
D.根据同位素的定义判断.
B.原子最外层电子数为2的元素可能为He、ⅡA族、ⅡB族等元素;
C.NaOH含有离子键和共价键;
D.根据同位素的定义判断.
解答:
解:A.元素的非金属性越强,对应的氢化物越稳定,还原性越弱,HF、HCl、HBr、HI的热稳定性以此减弱,还原性以此增强,故A错误;
B.原子最外层电子数为2的元素可能为He、ⅡA族、ⅡB族等元素,故B错误;
C.NaOH含有离子键和共价键,Na2O只含有离子键,故C错误;
D.
Sm与
Sm具有相同的质子数,但中子数不同,互为同位素,故D正确.
故选D.
B.原子最外层电子数为2的元素可能为He、ⅡA族、ⅡB族等元素,故B错误;
C.NaOH含有离子键和共价键,Na2O只含有离子键,故C错误;
D.
144 62 |
150 62 |
故选D.
点评:本题考查较为综合,涉及元素周期律、周期表、化学键以及原子结构等知识,为高频考点,侧重于学生的分析能力和基础知识的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
试判断C5H12O的同分异构体的种数( )
| A、8 | B、10 | C、13 | D、14 |
判断下列化合物中标出的显正价的元素正确的是( )
| A、OF2(F显正价) |
| B、CN-离子(N显正价) |
| C、NH3(H显正价) |
| D、SiC (C显正价) |
下列说法中不正确的是( )
| A、同系物的化学性质相似 |
| B、甲烷和环丙烷是同系物 |
| C、相对分子质量相同的几种化合物不一定互为同分异构体 |
| D、分子组成相差若干个CH2原子团的有机物不一定是同系物 |
某烃的结构简式为(CH3)2C=C(CH3)C≡CCH3,下列有关该烃的叙述正确的是( )
| A、分子中一定共平面的原子有12个 |
| B、分子中可能共平面的原子最多有16个 |
| C、分子中所有的碳原子一定共平面 |
| D、分子中一定共直线的原子有5个 |
某强酸性溶液X中还可能含有Fe2+、Al3+、NH4+、AlO2-、CO32-、SO42-,SiO32-、Cl-、H2SO3中的若干种,现取X溶液进行连续实验,实验过程及产物如下:

下列说法上正确的是( )

下列说法上正确的是( )
| A、由实验①可知,气体A一定是NO,沉淀C一定是BaSO4,原溶液中肯定含有Fe2+ |
| B、由实验②可知,气体D一定是NH3,原溶液中肯定含有NH4+,肯定不含Al3+ |
| C、由实验③可知,沉淀G可能是Al(OH)3和BaCO3 |
| D、原溶液中肯定含有Al3+,NH4+、H2SO3不能确定是否含有SO42- |
通常情况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NCl3的有关叙述正确的是( )
| A、分子中的所有原子均达到8电子稳定结构 |
| B、分子中N-C1键键长与CCl4分子中C-Cl键键长相等 |
| C、NCl3分子是平面三角形非极性分子 |
| D、NBr3比NCl3易挥发 |
下列生活中遇到的问题,不涉及到化学变化的是( )
| A、用CCl4可擦去圆珠笔油渍 |
| B、蜂蚁螯咬处涂抹稀氨水可减痛 |
| C、烹鱼时加入少量食醋和黄酒来调味 |
| D、用食醋来除水壶里的水垢 |
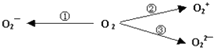 据2004年1月17日网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子
据2004年1月17日网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子